Кардиомиопатии
Кардиомиопатии — общее название группы заболеваний, характеризующихся структурными изменениями миокарда. Кардиомиопатии нередко приводят к развитию сердечной недостаточности, и хотя в некоторых случаях удается выяснить причины дисфункции миокарда, чаще всего этиология болезни остается неизвестной. К этой группе заболеваний не относятся поражения миокарда вследствие артериальной гипертензии, ишемической болезни сердца или пороков сердца.
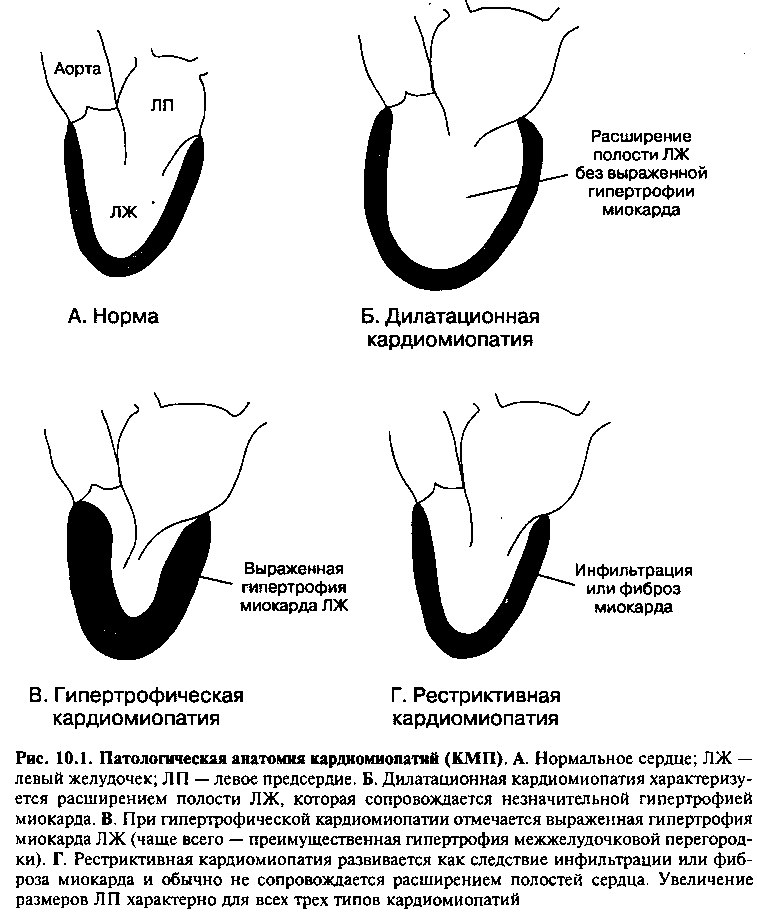
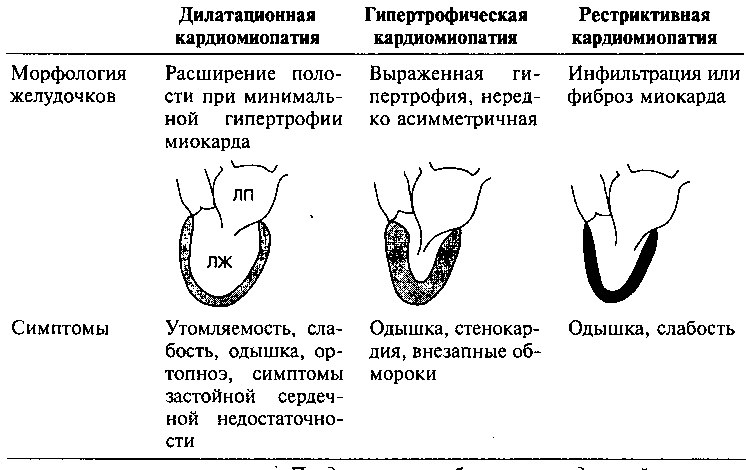
В зависимости от анатомических и физиологических изменений левого желудочка (ЛЖ) сердца различают три формы кардиопатий (рис. 10.1). Дилатационная кардиомиопатия характеризуется увеличением размеров полости и снижением систолической (сократительной) функции ЛЖ; гипертрофическая кардиомиопатия — утолщением стенок и нарушением диастолического расслабления ЛЖ; рестриктивная кардиомиопатия — увеличением жесткости (снижением эластичности) миокарда ЛЖ (вследствие фиброза или инфильтрации), при этом нарушается диастолическое расслабление, но систолическая функция ЛЖ, как правило, сохранена.
ДИЛАТАЦИОННАЯ КАРДИОМИОПАТИЯ (ДКМП)
Этиология
Увеличение размеров сердца при ДКМП обусловлено, в основном, расширением полости желудочков; степень гипертрофии миокарда при ДКМП, как правило, минимальна. Повреждение кардиомиоцитов, приводящее к развитию ДКМП, может быть следствием действия токсических факторов, нарушения метаболических процессов или инфекции (таблица 10.1). В большинстве случаев этиология ДКМП остается не выясненной («идиопатическая» ДКМП), однако причиной этого заболевания нередко является вирусный миокардит и хронический алкоголизм; кроме того, выделяется семейная форма ДКМП.
Острый вирусный миокардит обычно наблюдается у молодых, ранее не болевших лиц. Чаще всего возбудителем этого заболевания являются вирусы Коксаки группы В или эховирусы. Как правило, вирусный миокардит заканчивается полным выздоровлением, но по неизвестным причинам у некоторых больных может прогрессировать до ДКМП. Полагают, что поражение и фиброз миокарда у больных этой категории обусловлены активацией иммунных механизмов под действием компонентов вируса. Вместе с тем, терапия иммунодепрессантами не улучшает прогноза у больных вирусным миокардитом. Анализ образцов, полученных при трансвенозной биопсии миокарда правого желудочка (ПЖ), свидетельствует о том, что вирусный миокардит нередко сопровождается острой воспалительной реакцией, а у некоторых больных в миокарде выявляют РНК вируса Коксаки В.
Алкогольная кардиомиопатия развивается у лиц, хронически злоупотребляющих алкоголем. Патофизиология алкогольной кардиомиопатии неизвестна, однако этанол может нарушать функции клеток, ингибируя
процессы окислительного фосфорилирования и 0-окисления жирных кислот в митохондриях. Клинические и гистологические признаки алкогольной и дилатационной кардиомиопатий во многом схожи, но установление диагноза алкогольной кардиомиопатии имеет большое практическое значение, поскольку это одно из немногих потенциально обратимых состояний, при котором полный отказ от употребления алкоголя способствует значительному улучшению функции ЛЖ.
Патологическая анатомия
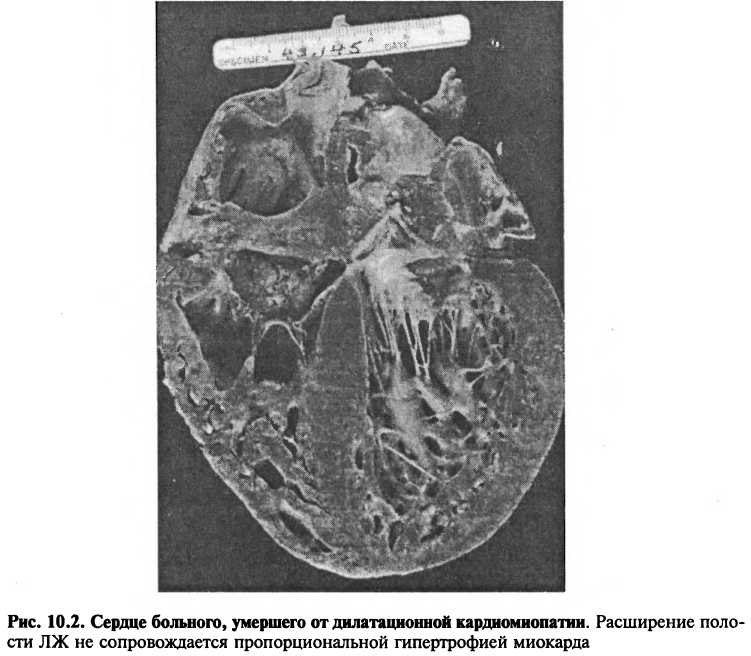
Дилатационная кардиомиопатия характеризуется расширением всех полостей сердца (рис. 10.2), хотя у некоторых больных может отмечаться увеличение только правых или левых отделов. Стенка ЛЖ несколько утолщена, однако дилатация полости желудочка не сопровождается пропорциональной гипертрофией миокарда. При микроскопическом исследовании выявляют признаки дегенерации кардиомиоцитов, нерегулярную гипертрофию и атрофию миофибрилл, нередко — выраженный интерстициальный и периваскулярный фиброз.
Патофизиология
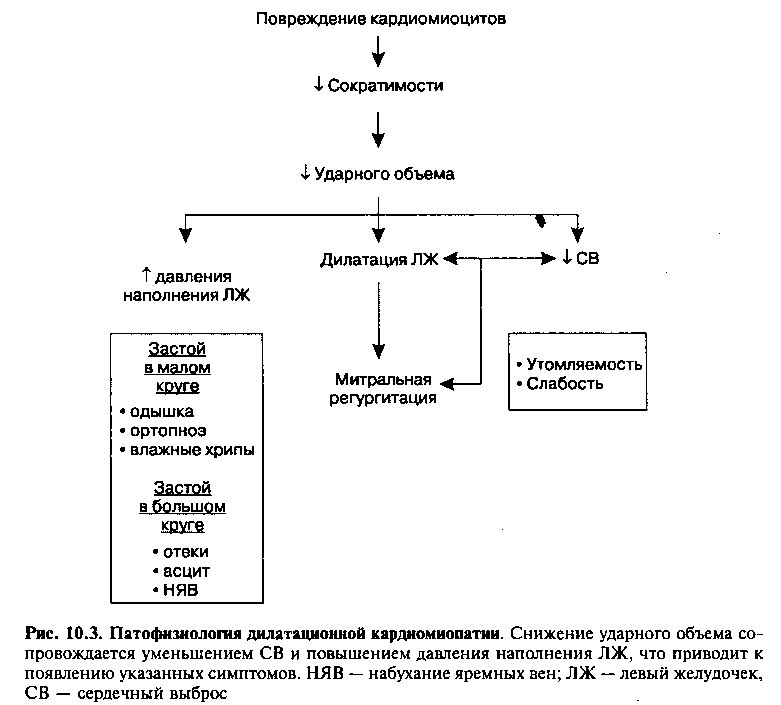
Основным клиническим проявлением ДКМП является дисфункция желудочков сердца и снижение сократимости миокарда (рис. 10.3). При ДКМП обычно поражены оба желудочка, но иногда встречается изолированная дисфункция ЛЖ и несколько реже — ПЖ.
Снижение ударного объема и сердечного выброса (СВ) вследствие нарушения сократимости миокарда сопровождается активацией двух компенсаторных механизмов: 1) механизма Франка—Старлинга (согласно которому, сила сокращений волокон миокарда усиливается пропорционально увеличению конечно-диастолического объема ЛЖ) и 2) стимуляции нейроэндокринных систем, которая первоначально обусловлена активацией симпатической нервной системы (глава 9). Повышение симпатического тонуса приводит к увеличению частоты сердечных сокращений и усилению сократимости миокарда, что способствует поддержанию СВ. Благодаря этим компенсаторным механизмам на начальных стадиях дисфункции желудочков заболевание может протекать бессимптомно, однако по мере дегенерации кардиомиоцитов и увеличения перегрузки объемом у больных возникают клинические симптомы сердечной недостаточности.
Снижение СВ и, как следствие, ухудшение кровоснабжения почек приводят к увеличению продукции ренина юкстагломерулярными клетками. При активации ренин-ангиотензиновой системы повышается общее периферическое сосудистое сопротивление (под действием ангиотензина II) и увеличивается объем циркулирующей крови (в связи с повышением уровня альдостерона). Как отмечалось в главе 9, эти эффекты первоначально противодействуют снижению СВ.
В дальнейшем нейроэндокринные «компенсаторные» реакции неизбежно приводят к ухудшению состояния больных. Так, при сужении артериолярного русла и повышении общего периферического сосудистого сопротивления (ОПСС) ЛЖ должен создавать большее усилие для выброса крови во время систолы. Увеличение объема циркулирующей крови (ОЦК) также Приводит к усилению нагрузки на ЛЖ и увеличению венозного возврата, что может сопровождаться застоем в малом и большом круге кровообращения.
Более того, дилатация полостей желудочков, усиливающаяся по мере прогрессирования кардиомиопатии, может быть причиной неполного захлопывания трикуспидального и митрального клапанов во время систолы и возникновения клапанной регургитации. Неблагоприятные последствия клапанной регургитации включают 1) перегрузку предсердий давлением и объемом, что сопровождается дилатацией предсердий и увеличением риска мерцательной аритмии; 2) уменьшение объема крови, выбрасываемой в аорту и поступающей в системную циркуляцию за счет регургитации части крови в левое предсердие.
Таблица 10.1. Причины развития дилатационной кардиомиопатии
Идиопатическая форма
Воспаление
Инфекционное (в первую очередь — вирусное)
Неинфекционное
Заболевание соединительной ткани
Перипартальная кардиомиопатия
Саркоидоз
Токсические факторы
Злоупотребление алкоголем
Химиотерапия (например, адриамицином)
Метаболические нарушения
Гипотиреоз
Хроническая гипокальциемия или гипофосфатемия
Нейро-мышечные нарушения
Мышечная или миотоническая дистрофия
Клиническая картина
Дилатационная кардиомиопатия проявляется, в основном, сердечной недостаточностью. Типичные симптомы, свидетельствующие о низком СВ, — это слабость, головокружение, одышка при нагрузке вследствие недостаточной перфузии тканей. Застой в легких приводит к одышке, ортопноэ, ночным приступам сердечной астмы, а застой в большом круге кровообращения — к появлению периферических отеков. Эти симптомы могут развиваться незаметно, и больные нередко жалуются только на увеличение массы тела (вследствие интерстициальных отеков) и одышку после нагрузки.
Физикальное обследование
У больных этой категории нередко отмечаются типичные симптомы низкого СВ: холодные бледные конечности (вследствие сужения периферических сосудов), низкое артериальное давление и тахикардия. Появление влажных хрипов указывает на застой в легочных венах, а притупление перкуторного звука в базальных отделах легких — на плевральный выпот. Размеры сердца увеличены, пальпаторно определяется ослабленный смещенный влево, разлитой верхушечный толчок, при аускультации выслушивается протодиастолический галоп, указывающий на систолическую дисфункцию ЛЖ. При выраженной дилатации ЛЖ нередко выслушивают шум митральной недостаточности. Правожелудочковая недостаточность характеризуется симптомами застоя в системных венах, набуханием шейных вен, гепатомегалией, асцитом и периферическими отеками. Увеличение полости ПЖ и нарушение сократимости миокарда часто сопровождаются трикуспидальной недостаточностью.
Инструментальные исследования
Рентгенография грудной клетки выявляет увеличение тени сердца. При развитии сердечной недостаточности изменяется легочный сосудистый рисунок, появляются признаки интерстициального и альвеолярного отека и плеврального выпота (рис. 3.5).
Изменения ЭЛТ обычно указывают на увеличение предсердий и желудочков сердца. Очаговый фиброз миокарда обусловливает развитие разнообразных аритмий (наиболее значимыми из них являются — мерцательная аритмия и желудочковая тахикардия). У большинства больных отмечаются нарушения проводимости (блокада правой или левой ножек пучка Гиса). Типичны нарушения реполяризации желудочков (изменение сегмента ST, зубца Т). Кроме того, в участках выраженного фиброза миокарда могут формироваться патологические зубцы Q, напоминающие зубцы Q при инфаркте миокарда.
Результаты эхокардиографического (ЭхоКГ) исследования имеют большое значение в диагностике этого заболевания. Эхокардиографическое исследование выявляет увеличение всех полостей сердца, выраженное нарушение сократимости ЛЖ, митральную и/или трикуспидальную регургитацию. В некоторых клиниках для оценки дилатации полостей сердца и количественного определения фракции выброса ЛЖ в дополнение или вместо ЭхоКГ проводят изотопную вентрикулографию (глава 3).
Катетеризация сердца позволяет выяснить, является ли дисфункция желудочков следствием ишемической болезни сердца. Эта процедура в первую очередь показана больным, у которых отмечаются приступы стенокардии или имеются электрокардиографические признаки перенесенного инфаркта миокарда. Анализ показателей гемодинамики обычно указывает на повышение диастолического давления в правых и левых отделах сердца (вследствие неполного освобождения полостей желудочков во время систолы), а также — на выраженное снижение СВ. Во время катетеризации сердца иногда проводят трансвенозную биопсию миокарда правого желудочка (для выявления этиологии ДКМП). Диагностическое значение биопсии миокарда у больных с ДКМП ограничено, и ее результаты лишь в редких случаях позволяют подобрать более эффективный способ лечения.
Лечение
Цель лечения больных с ДКМП заключается в устранении клинических симптомов и профилактике тяжелых осложнений этого заболевания, повышении качества и увеличении продолжительности жизни. Следовательно, проводимая терапия должна быть направлена на 1) устранение основного заболевания (если такое заболевание диагностировано); 2) профилактику прогрессирования дилатации желудочков сердца, 3) уменьшение выраженности застоя в малом и большом кругах кровообращения; 4) увеличение СВ; 5) профилактику угрожающих жизни аритмий и 6) тромбоэмболий, а также 7) решение вопроса о необходимости пересадки сердца.
Терапевтические мероприятия, направленные на уменьшение выраженности застоя и увеличение СВ, подробно обсуждались в главе, посвященной сердечной недостаточности (глава 9). Вначале ограничивают потребление поваренной соли и назначают больным этой категории диуретические препараты. Одним из наиболее значительных достижений последних 20 лет следует признать внедрение в клиническую практику препаратов, обладающих вазодилатирующим действием. Так, длительная терапия пероральными ингибиторами ангиотензинпревращающего фермента (АПФ) или гидралазином (вазодилататор, непосредственно влияющий на гладкие мышцы артериол) в сочетании с изосорбида динитратом (венодилататор) способствует нормализации показателей гемодинамики, повышению качества и увеличению продолжительности жизни больных этой категории. Результаты клинических исследований свидетельствуют о том, что терапия ингибиторами АПФ эффективна даже в тех случаях, когда у больных отсутствуют явные клинические симптомы дисфункции ЛЖ, поскольку предотвращает развитие симптомов сердечной недостаточности. Ингибиторы АПФ являются препаратами первого выбора при лечении больных с ДКМП. Комбинированная терапия гидралазином и изосорбида динитратом показана больным, плохо переносящим ингибиторы АПФ. В некоторых случаях больным с ДКМП для улучшения симптоматики назначают сердечные гликозиды, однако прием этих препаратов не сопровождается достоверным увеличением продолжительности жизни.
При развернутой форме ДКМП нередко отмечаются предсердные и желудочковые аритмии — в 40% случаев причиной смерти больных этой категории является желудочковая тахикардия и фибрилляция желудочка. Для предотвращения развития угрожающих жизни аритмий, особенно на фоне терапии диуретиками, крайне важно поддерживать уровень электролитов сыворотки крови в пределах нормальных значений (в первую очередь — концентрацию ионов натрия и магния). Результаты клинических исследований указывают на то, что антиаритмические средства, к сожалению, неэффективны в снижении смертности больных с ДКМП от желудочковых аритмий. Более того, назначение препаратов этого класса больным с выраженной дисфункцией ЛЖ может сопровождаться более выраженными нарушениями сердечного ритма (глава 17). В настоящее время единственно эффективным методом, позволяющим уменьшить риск смерти у больных с ДКМП и тяжелыми желудочковыми аритмиями, является имплантация автоматического дефибриллятора.
Стаз крови в плохо сокращающихся желудочках часто приводит к образованию пристеночных тромбов. Тромб, образовавшийся в ПЖ, может вызвать тромбоэмболию легочной артерии, а тромбы из ЛЖ — эмболии любых системных артерий с развитием инфаркта головного мозга, миокарда, почки и пр. Очевидно, что больным с ДКМП и тяжелой дисфункцией ЛЖ (фракция выброса < 30%) показаны пероральные антикоагулянты (например, варфарин). Вместе с тем, эффективность (или риск) длительной терапии антикоагулянтами у больных с ДКМП пока не подтверждена результатами проспективных клинических исследований.
В главе 9 отмечалось, что на фоне приема p-адреноблокаторов у больных ДКМП могут улучшаться симптомы заболевания и увеличиваться толерантность к физическим нагрузкам. Механизм этого положительного действия p-адреноблокаторов точно не известен. Усиление симпатического тонуса и стойкое повышение уровня катехоламинов в крови при ДКМП неблагоприятно влияет на структурные и функциональные свойства кардиомиоцитов. Известно, что у больных ДКМП снижено количество р,-адренорецепторов в миокарде, по-видимому, вследствие длительной гиперактивности симпатической нервной системы. Полагают, что положительный эффект p-адреноблокаторов обусловлен снижением симпатического тонуса и увеличением количества Pj-адренорецепторов в миокарде по принципу обратной связи. В настоящее время эффективность использования p-адреноблокаторов при лечении больных ДКМП остается предметом клинических исследований.
Некоторым больным с тяжелой формой застойной сердечной недостаточности показана пересадка сердца. Известно, что больные, которым была проведена пересадка сердца, имеют достоверно более благоприятный 5-летний прогноз, чем лица, получавшие традиционную медикаментозную терапию. Так, 5- и 10-летняя выживаемость больных после пересадки сердца составляет 74 и 55%. Вместе с тем, широкое распространение этого метода ограничено в связи с нехваткой донорских органов: ежегодно проводится менее чем 2500 пересадок сердца, тогда как количество больных, нуждающихся в этой операции, превышает 20000.
Прогноз
Несмотря на новые, более совершенные методы терапии, прогноз у больных ДКМП, которым не проводилась пересадка сердца, в целом, неблагоприятный и прямо зависит от тяжести дисфункции ЛЖ. Так, 5-летняя выживаемость больных, получающих только медикаментозную терапию, не превышает 50%. Поиск эффективных методов ранней профилактики, способных замедлить прогрессирование заболевания у больных с бессимптомной или легкой формой ДКМП и предупредить их внезапную смерть, является одним из основных направлений современных научных исследований в кардиологии.
ГИПЕРТРОФИЧЕСКАЯ КАРДИОМИОПАТИЯ
В специальной литературе гипертрофической кардиомиопатии (ГКМП) иногда уделяют особое внимание, поскольку это одна из наиболее часто встречающихся патологий сердца у спортсменов молодого возраста, внезапно умерших во время тяжелой физической нагрузки. Для ГКМП характерна выраженная гипертрофия ЛЖ, не связанная с постоянной перегрузкой ЛЖ давлением (например, вследствие артериальной гипертензии или аортального стеноза). Другие термины, применяемые для обозначения этого заболевания: гипертрофическая обструктивная кардиомиопатия (ГОКМ) и идиопатический гипертрофический субаортальный стеноз (ИГСС). При ГКМП сократимость ЛЖ усилена, однако вследствие гипертрофии и увеличения жесткости стенок нарушено диастолическое расслабление и повышено диастолическое давление.
Этиология
Гипертрофическая кардиомиопатия может быть наследственной или развиваться спорадически. Полагают, что ГКМП наследуется по аутосомно-доминантному типу с различной пенетрантностью. Семейная (наследственная) форма ГКМП является гетерогенной, известны не менее 5 генов, мутации которых могут приводить к развитию этого заболевания. Выделены белки, кодируемые тремя из этих генов: тяжелая 0-цепь миозина (0-МНС), сердечный тропин Т и а-тропомиозин. По существующим оценкам, мутации в локусах, кодирующих эти саркомерные белки, обусловливают до 70% случаев семейной ГКМП.
Патофизиология и течение семейной ГКМП могут варьировать в широких пределах, причем это зависит в большей степени от особенностей мутации, а не от того, в каком из 5 известных генов она произошла. Так, клиническое течение заболевания при мутациях генов 0-МНС и тропонина Т практически не различается. Напротив, две разные мутации гена Р-МНС могут сопровождаться развитием ГКМП различной степени выраженности, сопряженной с разной летальностью.
По данным клинических исследований, прогноз у больных с семейной ГКМП также в значительной степени зависит от характера мутации. Например, мутации гена р-МНС, при которых нарушается аминокислотный состав кодируемого белка, обусловливают более высокую летальность, чем мутации, не приводящие к изменению аминокислотного состава.
Патологическая анатомия
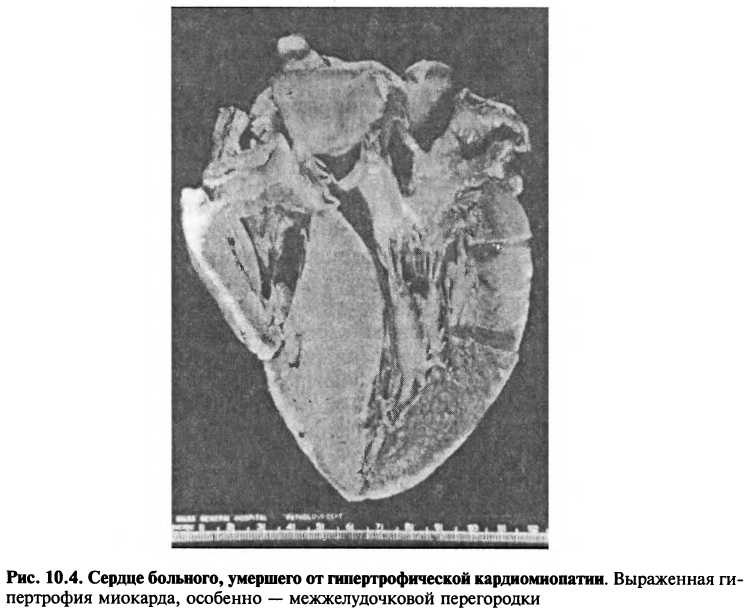
Хотя при ГКМП может наблюдаться гипертрофия любых отделов желудочков, чаще всего (90% случаев) выявляют асимметричную гипертрофию межжелудочковой перегородки (рис. 10.4). У некоторых больных отмечается равномерная концентрическая гипертрофия левого и правого желудочков, локальная гипертрофия средних отделов или верхушки ЛЖ.
Гистологические изменения при ГКМП существенно отличаются от изменений при гипертрофии желудочков вследствие артериальной гипертензии, которая характеризуется равномерным утолщением и упорядоченным расположением миофибрилл. При ГКМП взаимное расположение миофибрилл нарушено (рис. 10.5): короткие, гипертрофированные миофибриллы расположены беспорядочно и окружены рыхлой соединитель-
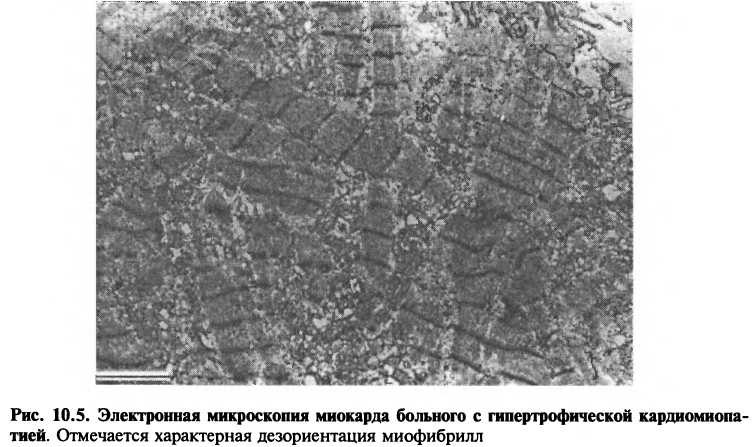
ной тканью. Полагают, что дезориентация миофибрилл может быть одной из причин нарушения диастолического расслабления и возникновения аритмий, типичных для больных этой категории.
Патофизиология
Основной патофизиологический признак ГКМП — выраженное снижение расслабления и эластичности ЛЖ, а также уменьшение наполнения ЛЖ, вследствие выраженной гипертрофии миокарда (рис. 10.6). Кроме того, у больных с асимметричной гипертрофией верхних отделов межжелудочковой перегородки иногда наблюдаются нарушения, обусловленные преходящей обструкцией выносящего тракта ЛЖ во время систолы. Полагают, что возникновение обструкции обусловлено выбуханием гипертрофированной межжелудочковой перегородки в сторону выносящего тракта ЛЖ и патологическим движением передней створки митрального клапана в ту же сторону (рис. 10.7). Механизм этого явления объясняется следующим: 1) во время систолы скорость движения крови вдоль верхних отделов межжелудочковой перегородки увеличивается вследствие сужения выносящего тракта ЛЖ (из-за гипертрофии межжелудочковой перегородки); 2) при увеличении скорости кровотока создается градиент давления между полостью и выносящим трактом ЛЖ, который «притягивает» переднюю створку митрального клапана к межжелудочковой перегородке; 3) передняя створка митрального клапана приближается к гипертрофированной межжелудочковой перегородке, на время перекрывая поступление крови в аорту.
На практике целесообразно различать две патофизиологические формы ГКМП: обструктивную и необструктивную.
НЕОБСТРУКТИВНАЯ ГКМП
Сократимость ЛЖ при ГКМП, как правило, усилена, однако гипертрофия миокарда сопровождается увеличением жесткости стенок ЛЖ и нарушением диастолического расслабления желудочка. Снижение эластичности ЛЖ приводит к нарушению нормальной взаимосвязи между диастолическим давлением и объемом, при этом кривая диастолического давления наполнения смещается вверх (рис. 9.7Б). Высокое диастолическое давление в ЛЖ сопровождается повышением давления в левом предсердии, легочных венах и капиллярах. Как следствие, типичным клиническим проявлением этой формы заболевания является одышка при нагрузке.

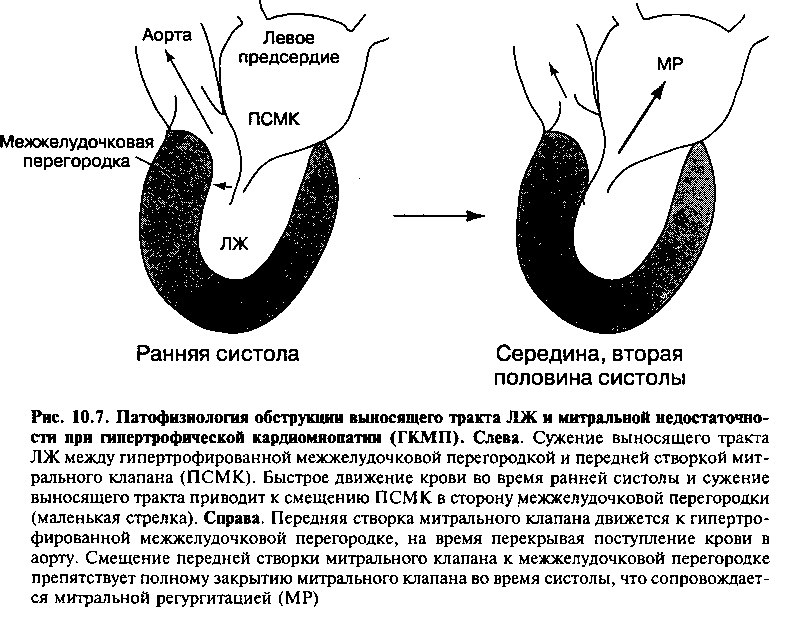
ОБСТРУКТИВНАЯ ГКМП
Повышение давления в левом предсердии и легочных капиллярах у больных этой категории обусловлено как снижением эластичности, так и обструкцией выносящего тракта ЛЖ. Градиент давления, возникающий между полостью и выносящим трактом ЛЖ дистальнее места обструкции, приводит к повышению напряжения в стенке желудочка и увеличению потребности миокарда в кислороде, следствием чего могут быть приступы стенокардии (рис. 10.6). Кроме того, смещение передней створки митрального клапана к межжелудочковой перегородке (и, следовательно, в сторону от задней створки клапана) препятствует полному закрытию митрального клапана во время систолы, что сопровождается митральной регургитацией. Митральная регургитация приводит к дальнейшему повышению давления в левом предсердии и легочных венах, что только усиливает одышку.
Градиент систолического давления при обструктивной ГКМП является «динамическим»: его величина изменяется во время сокращения желудочка и в любой момент зависит от расстояния между передней створкой митрального клапана и гипертрофированной межжелудочковой перегородкой. Очевидно, что состояния, сопровождающиеся уменьшением объема полости ЛЖ (например, при снижении венозного возврата вследствие уменьшения ОЦК), будут сопровождаться более выраженной обструкцией выносящего тракта ЛЖ, т. к. в этом случае передняя створка митрального клапана приближается к межжелудочковой перегородке. Такой же эффект оказывают препараты с положительным инотропным действием (усиливающие силу сокращений ЛЖ). Препараты, обладающие отрицательным инотропным действием (например, 0-адреноблокаторы), напротив, уменьшают обструкцию выносящего тракта ЛЖ.
Хотя обструкция выносящего тракта ЛЖ во время систолы сопровождается появлением характерных шумов, основные клинические симптомы как обструктивной, так и необструктивной ГКМП обусловлены уменьшением эластичности и диастолической дисфункцией ЛЖ.
Клиническая картина
Течение ГКМП варьирует от бессимптомного до тяжелого, в значительной степени ограничивающего физическую активность больных. Средний возраст начала ГКМП — 25 лет.
Типичный симптом ГКМП — одышка вследствие повышения диастолического давления в ЛЖ (и, следовательно, давления в легочных капиллярах). Кроме того, одышка усугубляется за счет повышеного систолического давления в ЛЖ и митральной регургитации, наблюдающейся у больных с обструктивной ГКМП.
У больных с ГКМП даже в отсутствие изменений коронарных артерий нередко возникают приступы стенокардии. Полагают, что причиной ишемии миокарда в этих случаях может быть: 1) повышение потребности гипертрофированного миокарда в кислороде и 2) утолщение стенки и сужение просвета мелких ветвей коронарных артерий, кровоснабжающих участки гипертрофированного миокарда (эти ветви коронарных артерий частично утрачивают способность к расширению, что сопровождается недостаточным поступлением кислорода в миокард). Повышение систолического давления ЛЖ при обструкции выносящего тракта и, как следствие, увеличение напряжения стенки желудочка также сопряжено с дополнительным количеством кислорода.
Причиной обмороков у больных с ГКМП могут быть аритмии, развивающиеся вследствие нарушения структуры миофибрилл (см. далее). У больных с обструктивной ГКМП обмороки нередко наблюдаются на фоне физической нагрузки, когда усиленные сокращения ЛЖ приводят к образованию большого градиента давления и преходящему снижению СВ. Для больных с обструктивной ГКМП типично так же ортостатическое головокружение. Причина этого явления заключается в том, что при вертикальном положении тела кровь под действием силы тяжести скапливается в нижних конечностях, уменьшаются венозный возврат и размеры ЛЖ, усиливается обструкция выносящего тракта ЛЖ, снижается СВ и кровоснабжение головного мозга.
К сожалению, первым проявлением ГКМП может быть внезапная смерть больного вследствие фибрилляции желудочков — особенно лиц молодого возраста во время интенсивных физических нагрузок.
Физикальное обследование
Легкая форма ГКМП может протекать бессимптомно, и при физикальном обследовании больных этой категории отклонений от нормы не обнаруживают. Тем не менее, типичным клиническим признаком ГКМП является появление IV сердечного тона (S4), возникающего при сокращении левого предсердия и поступлении крови в ЛЖ, стенки которого частично утратили эластичность (глава 2). Кроме того, при пальпации грудной клетки можно обнаружить пресистолический («двойной») верхушечный толчок, возникающий в результате усиленного сокращения предсердий.
При обструктивной ГКМП почти всегда обнаруживают дикротический пульс на сонной артерии (быстрое ускорение пульса во время ранней систолы с последующим быстрым замедлением при наличии обструкции выносящего тракта ЛЖ). Другой типичный признак обструкции выносящего тракта — систолическое дрожание типа крещендо-декрещендо вдоль левого края рукоятки грудины (вследствие турбулентного тока крови через суженный выносящий тракт ЛЖ). При аускультации нередко обнаруживают изолированный пансистолический шум митральной недостаточности, наиболее выраженный на верхушке. Систолический шум изгнания усиливается во время проб, увеличивающих сократимость, уменьшающих преднагрузку или постнагрузку (таблица 10.2). Эти аускультативные пробы нередко облегчают дифференциальную диагностику шумов (например, при ГКМП и аортальном стенозе).
Таблица 10.2. Изменение систолического шума изгнания на фоне аускультативных проб у больных с аортальным стенозом и ГКМП
Проба Вальсальвы |
Приседание на корточки |
Переход в положение стоя |
|
Преднагрузка |
4 |
т |
г |
Постнагрузка |
ф |
г |
|
Шум при ГКМП |
т |
г |
т |
Шум аортального стеноза |
г |
Т (обычно) |
г |
Инструментальные исследования
К типичным изменениям ЭЛТ при ГКМП относят признаки гипертрофии ЛЖ и глубокие зубцы Q в передних и боковых отведениях, отражающие начало процесса деполяризации гипертрофированной межжелудочковой перегородки. У больных этой категории часто возникают угрожающие жизни желудочковые и предсердные аритмии. Больные ГКМП плохо переносят мерцательную аритмию, так как при ней СВ может снижаться почти на 25%, поскольку утративший эластичность ЛЖ перестает получать дополнительный объем крови в систему предсердий. Наиболее опасны желудочковые аритмии, следствием которых может быть фибрилляция желудочков и внезапная смерть больного, даже если ранее у него не наблюдалось явных клинических признаков заболевания.
Эхокардиография — один из наиболее информативных методов диагностики ГКМП. Она позволяет выявить ассиметричную гипертрофию ЛЖ, обструкцию выносящего тракта ЛЖ, особенности движения митрального клапана (в направлении гипертрофированной межжелудочковой перегородки), среднесистолическое прикрытие аортального клапана (при движении крови через суженный выносящий тракт ЛЖ). Доплеровская ЭхоКГ является наиболее точным методом количественной оценки градиента кровотока и сопутствующей митральной регургитации. Детям и подросткам с легкой ГКМП эхокардиографическое исследование следует проводить периодически, т. к. в пубертатном периоде нередко наблюдается прогрессирование гипертрофии миокарда.
Катетеризация сердца показана в случае неясного диагноза или если планируется хирургическое вмешательство. Этот метод позволяет выявить градиент давления в выносящем тракте ЛЖ в покое или при функциональных пробах, сопровождающихся уменьшением размеров ЛЖ и провоцирующих обструкцию выносящего тракта. Биопсия миокарда во время катетеризации сердца необязательна, поскольку ее результаты малоинформативны при оценке тяжести или долгосрочного прогноза заболевания.
Генетическое тестирование больных с ГКМП в современной клинической практике не проводится, однако в будущем генотипирование может стать одним из наиболее эффективных неинвазивных методов диагностики и оценки риска заболевания у лиц с наследственной предрасположенностью к ГКМП.
Лечение
Препаратами первого выбора при лечении больных с ГКМП являются $-адреноблокаторы, которые 1) снижают потребность миокарда в кислороде, уменьшая частоту и силу сердечных сокращений (и, следовательно, препятствуют возникновению приступов стенокардии и ослабляют одышку); 2) уменьшают градиент давления в ЛЖ во время нагрузки, ослабляя силу сердечных сокращений и способствуя увеличению размеров полости желудочка (при этом увеличивается расстояние между передней створкой митрального клапана и межжелудочковой перегородкой); 3) подавляют желудочковую экстрасистолию. Несмотря на антиаритмический эффект, терапия 0-адреноблокаторами не способствует уменьшению риска внезапной смерти у больных этой категории.
Антагонисты кальция уменьшают жесткость стенок ЛЖ и в некоторых случаях, особенно при неэффективности p-адреноблокаторов, способствуют повышению толерантности к физическим нагрузкам. Антиаритмические средства подавляют желудочковые аритмии, однако терапия препаратами этого класса не снижает риск внезапной смерти у больных с ГКМП. По данным клинических исследований, наиболее эффективным антиарит-мическим средством является амиодарон (глава 17). Больные с ГКМП должны избегать тяжелых физических нагрузок и участия в спортивных соревнованиях в связи с высоким риском внезапной смерти. Больным, у которых наблюдаются угрожающие жизни аритмии (например, желудочковая тахикардия), показана имплантация автоматического кардиовертера-дефибриллятора.
У больных с обструктивной ГКМП может развиться инфекционный эндокардит, обусловленный турбулентным током крови через суженный выносящий тракт ЛЖ и митральной недостаточностью. Поэтому таким больным показана антибиотикопрофилакгика при любых хирургических вмешательствах, которые могут сопровождаться бактериемией (см. главу 8).
Хирургическое лечение {миомэктомия) показано больным, у которых медикаментозная терапия оказалась неэффективной. Во время операции часть гипертрофированного миокарда иссекают, что в большинстве случаев способствует ослаблению симптомов заболевания.
Результаты клинических исследований свидетельствуют о том, что состояние больных с обструктивной ГКМП может улучшаться после установки искусственного двухкамерного водителя ритма, электроды которого имплантируют в правое предсердие и правый желудочек. После установки искусственного водителя ритма уменьшается градиент давления в ЛЖ, по-видимому, в результате разобщения нормальной последовательности сокращений желудочка и увеличения расстояния между передней створкой митрального клапана и межжелудочковой перегородкой. Эта операция эффективна только у небольшой части больных.
Генетическое консультирование показано всем больным с ГКМП. Поскольку это заболевание наследуется по аутосомно-доминантному типу, риск передачи мутантного гена детям составляет 50%. Более того, всем родственникам больных первой степени родства необходимо провести эхокардиографическое исследование. Даже при отсутствии симптомов у пациентов с ГКМП повышен риск развития тяжелых осложнений (включая внезапную смерть), поэтому они должны находиться под наблюдением врача.
Прогноз
Частота внезапной смерти при ГКМП составляет 2—4% среди больных взрослого возраста и 4—6% — среди детей и подростков. Неблагоприятный прогноз у больных ГКМП определяется следующими факторами: молодым возрастом больного, наследственной формой ГКМП и наличием случаев внезапной смерти у родственников первой степени родства, указаниями на обмороки в анамнезе, эпизоды ишемии миокарда и желудочковые аритмии.
РЕСТРИКТИВНАЯ КАРДИОМИОПАТИЯ
Рестриктивные кардиомиопатии встречаются реже, чем ДКМП или ГКМП. Для них характерны выраженная ригидность стенок желудочков сердца (нередко — без гипертрофии миокарда) и нарушение диастолического наполнения при нормальной систолической функции. Причинами рестриктивных кардиомиопатий могут быть: 1) эндомиокардиальный фиброз или образование рубцовой ткани; 2) инфильтрация миокарда патологическими субстанциями, например, амилоидом (таблица 10.3).
Патофизиология
Фиброз или инфильтрация миокарда сопровождается снижением эластичности желудочков и приводит к смещению кривой пассивного диастолического наполнения вверх (рис. 9.7Б). Как следствие, внутрижелудочковое давление остается повышенным на протяжении всей диастолы, в результате чего 1) повышается давление в венах большого и малого кругов кровообращения, что приводит к появлению симптомов застоя в обоих кругах; 2) уменьшается размер полости ЛЖ (снижение ударного объема и СВ).
Таблица 10.3. Причины развития рестриктивной кардиомиопатии
Поражение миокарда |
Поражение эндокарда |
|
Неинфильтративное Идиопатическая Склеродермия Инфильтративное Амилоидоз Саркоидоз Болезни накопления Гемохроматоз Уменьшение запасов гликогена |
Эндомиокардиальный фиброз Гиперэозинофильный синдром Метастазы опухоли Лучевая терапия |
Клиническая картина
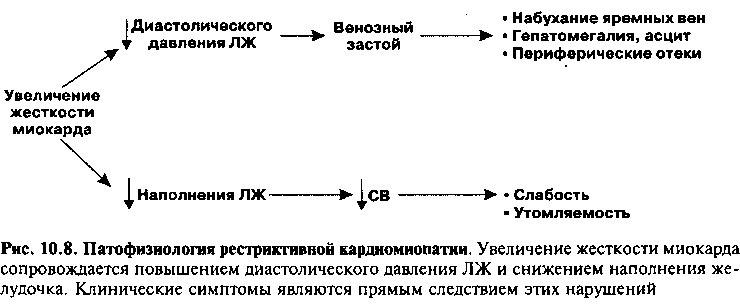
Учитывая патофизиологические механизмы развития рестриктивной кардиомиопатии, очевидно, что основными клиническими признаками этого заболевания являются симптомы право- и левожелудочковой недостаточности (рис. 10.8). Снижение СВ проявляется утомляемостью и сни-
жением толерантности к физическим нагрузкам. Застой в большом круге (нередко более выраженный, чем застой в малом круге) сопровождается набуханием шейных вен, периферическими отеками, асцитом, гепатомегалией и болезненностью в правом подреберье.
Инструментальные исследования
В главе 14 отмечается, что клинические проявления и характер нарушений гемодинамики при рестриктивной кардиомиопатии и констриктивном перикардите во многом схожи. Вместе с тем, дифференциальный диагноз между этими заболеваниями крайне важен, поскольку, в отличие от рестриктивной кардиомиопатии, констриктивный перикардит хорошо поддается лечению.
При дифференциальном диагнозе между рестриктивной кардиомиопатией и констриктивным перикардитом решающее значение имеют результаты трансвенозной биопсии эндомиокарда, компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ). Так, при рестриктивной кардиомиопатии анализ биоптатов эндомиокарда позволит выявить отложение в миокарде амилоида, гемохроматоз, метастатическое поражение и пр. Напротив, при КТ и МРТ можно обнаружить утолщение перикарда, типичное для констриктивного перикардита, но не рестриктивной кардиомиопатии.
Лечение
Прогноз при рестриктивной кардиомиопатии в отсутствии эффективной терапии основного заболевания обычно крайне неблагоприятный. Так, на ранних стадиях гемохроматоза эффективны флеботомия и терапия комплекснообразующими средствами. Симптоматическое лечение направлено на улучшение состояния больных, уменьшение застойных явлений в легких и включает ограничение потребления поваренной соли и назначение диуретиков под тщательным наблюдением врача. В отличие от ДКМП, применение сердечных гликозидов и вазодилататоров нецелесообразно, т. к. у больных этой категории систолическая функция ЛЖ, как правило, не нарушена. В некоторых случаях рестриктивная кардиомиопатия сопровождается образованием пристеночных тромбов в ЛЖ, и таким больным показан постоянный прием пероральных антикоагулянтов.
ЗАКЛЮЧЕНИЕ
1. В зависимости от патофизиологических особенностей поражения миокарда различают дилатационную, гипертрофическую и рестриктивную кардиомиопатию (таблица 10.4).
2. Дилатационная кардиомиопатия характеризуется расширением полости и систолической дисфункцией ЛЖ. Прогрессирующая дилатация полости левого желудочка часто приводит к сердечной недостаточности, желудочковым аритмиям и тромбоэмболиям. Терапия ингибиторами ангиотензинпревращающего фермента способствует улучшению долгосрочного прогноза у больных этой категории.
3. Гипертрофическая кардиомиопатия характеризуется выраженной гипертрофией миокарда и диастолической дисфункцией ЛЖ. Нередко наблюдается динамическая обструкция выносящего тракта ЛЖ во время систолы. Типичные симптомы — одышка и стенокардия напряжения. Желудочковые аритмии могут быть причиной внезапной смерти больных.
4. Рестриктивная кардиомиопатия — относительно редко встречающееся заболевание, характеризующееся нарушением диастолического расслабления желудочков вследствие инфильтрации или фиброза миокарда. Типичны симптомы сердечной недостаточности.
Таблица 10.4. Кардиомиопатии
Дилатационная |
Гипертрофическая |
Рестриктивная |
кардиомиопатия |
кардиомиопатия |
кардиомиопатия |
Физикальные данные |
Влажные хрипы в легких, S3, при правожелудочковой недостаточности: набухание яремных вен, гепатомегалия, периферические отеки |
S4, при обструкции выносящего тракта ЛЖ: систолический шум изгнания, наиболее выраженный вдоль левого края грудины, шум митральной недостаточности |
Признаки правожелудочковой недостаточности: набухание яремных вен, гепатомегалия, периферические отеки |
Патофизиология |
Нарушение систолической функции |
Нарушение диастолической функции, усиление систолической функции ЛЖ (нередко с динамической обструкцией) |
Нарушение диастолического расслабления при нормальной систолической функции |
Контуры тени сердца на рентгенограмме |
Увеличение |
Норма или увеличение |
Обычно норма |
ЭхоКГ |
Признаки дилатации, нарушение сократимости ЛЖ |
Гипертрофия ЛЖ, чаще — межжелудочковой перегородки; передне-систолическое движение передней створки МК, митральная регургитация |
Нормальная систолическая функция; неоднородный эхосигнал при инфильтративном поражении миокарда |