Регуляция сосудистого тонуса
Гладкая мускулатура сосудов
Так как метаболические потребности организма постоянно изменяются, сердечно-сосудистая система должна постоянно регулировать диаметр кровеносных сосудов. Целями этих постоянных изменений в сосудах являются: (1) регуляция скорости кровотока через отдельные ткани (функция артериол) и (2) регуляция распределения объема крови и наполнения камер сердца (функция вен). Эти изменения диаметра осуществляются посредство^регуляции сократительной активности гладкомышечных клеток, которые находятся в стенках всех сосудов за исключением капилляров. Задача гладкой мускулатуры сосудов представляется уникальной, поскольку для того, чтобы поддерживать определенную величину диаметра сосуда при наличии постоянного расширяющего давления крови в нем, гладкая мускулатура сосудов должна обладать способностью сохранять активное напряжение на протяжении длительного периода времени.
Существует много функциональных характеристик, которые отличают гладкую мускулатуру как от скелетной, так и сердечной мышцы. Например, по сравнению с другими типами мышц, гладкомышечные клетки
1) сокращаются и расслабляются гораздо более медленно,
2) развивают активное напряжение при большем диапазоне длины мышцы,
3) могут изменять свою сократительную активность, вследствие потенциалов действия или вследствие изменений мембранного потенциала покоя,
4) могут изменять свою сократительную активность при отсутствии изменений величины мембранного потенциала,
5) поддерживают напряжение на протяжении длительного времени при низких энергозатратах,
6) могут активироваться при растяжении.
Механика сокращения
Клетки гладкой мускулатуры сосудов невелики по размеру (около 5 мкм х 50 мкм), веретенообразной формы и циркулярно расположены в стенке сосудов. Во многих сосудах соседние гладкомышечные клетки электрически связаны с помощью вставочных дисков, сходных с теми, что обнаружены в миокарде.
Как и в других типах мышц, развитие силы и сокращения гладкой мышцы являются результатом взаимодействия с помощью поперечных мостиков между тонкими и толстыми сократительными нитями, состоящими из миозина и актина соответственно.
Однако в гладкой мышце эти волокна не образуют регулярных повторяющихся единиц саркомеров. Вследствие этого клетки «гладкой» мышцы утрачивают видимую под микроскопом исчерченность, характерную для скелетных и сердечных мышечных клеток. Нити актина в гладкой мышце гораздо длиннее, чем в поперечнополосатой мышце. Многие из этих нитей актина прикрепляются к внутренней поверхности клетки с помощью образований, которые называются плотными спайками. Внутри клетки нити актина соединены между собой небольшими связками поперечных структур, которые называются плотными тельцами. Нити миозина распределены между нитями актина гладкомышечной клетки в более случайном порядке по сравнению с регулярным чередованием, характерным для поперечнополосатых мышц. В поперечнополосатой мышце все без исключения сократительные нити расположены вдоль продольной оси клетки, в то время как в гладкой мышце многие сократительные нити направлены под углом или даже поперечно по отношению к продольной оси клетки. Несмотря на отсутствие организованных саркомеров, изменения длины гладкой мышцы влияют на ее способность к развитию активного напряжения. Возможно, благодаря наличию длинных нитей актина и отсутствию организованных саркомеров, гладкая мышца развивает напряжение в большем диапазоне длины, по сравнению со скелетной или сердечной мышцей.
Как и в поперечнополосатой мышце, сила взаимодействия поперечных мостиков между тонкими и толстыми нитями в гладкой мышце регулируется, прежде всего, изменением уровня свободного внутриклеточного Са2+, уровень которого колеблется приблизительно от 10’7 моль в релаксированной мышце до 10“6моль во время максимального сокращения. В то же время последовательность этапов сопряжения повышения уровня свободного Са2+ с взаимодействием сократительных нитей отличается в гладкой мышце от этапов в поперечнополосатой мышце. В гладкой мышце:
1. Са2+ сперва образует комплекс с кальций-связывающим белком, кальмодулином.
•2. Затем комплекс Са2+-кальмодулин активирует фосфорилирующий фермент, который называется киназой легкой цепи миозина.
3. Этот фермент вызывает фосфорилирование при участии аденозинтрифосфата (АТФ) легкой пептидной цепи, которая является частью головки поперечного мостика миозина.
4. Фосфорилирование легкой цепи миозина делает возможным образование поперечных мостиков и циклическое соединение, во время которого используется энергия АТФ для возникновения напряжения и укорочения мышцы.
Гладкая мышца представляет собой уникальное образование еще и потому, что если напряжение развилось, оно может поддерживаться при очень низких энергетических затратах, т.е. без потребности в постоянном расщеплении АТФ при циклическом образовании поперечных мостиков. Механизм, ответственный за данный процесс, до сих пор остается недостаточно изученным, но предположительно он заключается в очень медленном или даже нециклическом образовании поперечных мостиков. Он обычно называется защелкнутым мостиком и может включать дефосфорилирование легкой цепи прикрепленных поперечных мостиков. Также благодаря механизмам, все еще не до конца изученным, представляется, что сократительная активность гладкой мускулатуры сосудов регулируется посредством не только изменений уровня внутриклеточного Са2+, но и за счет изменения чувствительности сократительного аппарата к Са2+. Таким образом, сократительная способность гладких мышц сосудов может иногда изменяться при отсутствии изменений уровня свободного внутриклеточного Са2+.
Мембранные потенциалы
Клетки гладкой мускулатуры обладают мембранным потенциал покоя, величина которого колеблется от -40 до -65 мВ, что ниже, чем в поперечнополосатой мускулатуре. Как и во всех клетках, мембранный потенциал покоя гладкой мышцы преимущественно определяется степенью проницаемости для калия. В гладкой мышце обнаружено несколько типов калиевых каналов. Один из них, преимущественно ответственный за создание мембранного потенциала покоя, носит название К+ канала выпрямления, направленного внутрь. (Термин выпрямление, направленное внутрь, означает, что ионы К+ передвигаются в клетку через данный канал с большей легкостью, чем они выходят через него наружу). Кроме того, существует А ТФ-зависимый К+ канал, который закрыт при нормальном уровне АТФ в клетке и открывается при падении уровня АТФ. Данный канал может играть важную роль в приспособлении уровня органного кровотока к метаболическим потребностям ткани.
Потенциалы действия в клетках гладкой мышцы возникают регулярно только в определенных сосудах. Когда это происходит, потенциалы действия гладкой мышцы инициируются преимущественно потоком Са2+ внутрь клетки и развиваются медленно, подобно сердечным «медленно нарастающим» потенциалам действия (см. рис. 3-3). Как и в сердце, этот направленный внутрь (деполяризующий) поток Са2+ происходит через электроуправляемый кальциевый канал (ЭУКК), этот канал представляет собой один из типов кальциевых каналов, имеющихся в гладкой мускулатуре. Фаза реполяризации потенциала действия происходит преимущественно за счет выхода ионов калия, как через калиевые каналы медленного выпрямления, так и через активируемые кальцием калиевые каналы.
Кроме упомянутых, в гладкой мускулатуре сосудов обнаружены многие другие типы ионных каналов, но в большинстве случаев их конкретная роль в функции сердечно-сосудистой системы остается неизвестной. Например, существуют неселективные, реагирующие на растяжение каналы, которые могут участвовать в реакции гладкой мышцы на ее растяжение Однако читатель должен учитывать, что многие из важных ионных каналов в гладкой мускулатуре сосудов являются также важными и в сердечной мышце (см. табл 3-1).
Электромеханическое и фармакомеханическое сопряжение
В гладкой мышце изменения уровней внутриклеточного свободного Са2+ могут происходить как на фоне изменений мембранного потенциала, так и без них. Вовлеченные в данный процесс механизмы называются электромеханическим и фармако-механическим сопряжением соответственно и представлены на рнс. 8-1.
Электромеханическое сопряжение, представленное на левой половине рис. 8-1 осуществляется, так как поверхностная мембрана гладкой мышцы содержит электро- * управляемые кальциевые каналы (тот же тип ЭУКК, который принимает участие в | образовании потенциала действия). Деполяризация мембраны увеличивает вероятность 1 открытия данных каналов и таким образом приводит к сокращению гладкомышечных 1 клеток и сужению сосудов. Наоборот, гиперполяризация мембраны приводит к рас- J слаблению гладкой мышцы и расширению сосудов. Поскольку ЭУККдля Са2+ частич- 1 но активируется низким значения мембранным потенциалом покоя гладкой мускула- 1 туры сосудов, изменения потенциала покоя могут привести к изменениям скорости ч входа кальция в покое, а следовательно, базального состояния сократимости. 1
При фармакомеханическом сопряжении химические факторы (например, освобож- | дение нейромедиаторов) могут индуцировать сокращение гладкой мышцы без потребно- 1 сти в изменении мембранного потенциала Как показано в правой части рис. 8-1, взаи-1 модействие вазоконстрикторов (таких как норадреналин) со специфическим | рецептором мембраны (таким как а-адренорецептор) запускает процесс, который при-1 водит к увеличению уровня свободного внутриклеточного Са2+ по двум причинам. Одна! заключается в том, что активированный рецептор может открыть хемоуправляемыеъ кальциевые каналы (ХУК) поверхностной мембраны, что приводит к поступлению! Са2+ из внеклеточной жидкости. Другая — в том, что активированный рецептор может! стимулировать образование внутриклеточного «вторичного медиатора», инозинтри-1
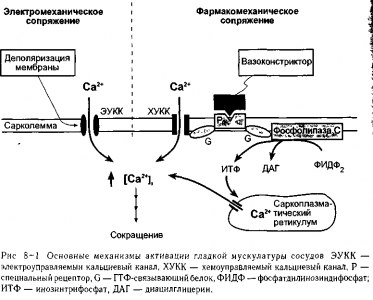
фосфата (ИТф),моторый открывает специфические каналы, через которые происходит освобождение Са2* из депо внутриклеточного саркоплазматического ретикулума. В обоих случаях активированный рецептор сперва стимулирует специфические гуано-зинтрифосфат-связывающие белки (ГТФ-связывающие белки или протеины G).
Читателю не следует делать вывод из рис. 8-1, что все вазоактивные химические факторы (химические агенты, которые вызывают сосудистые эффекты) оказывают свое действие на гладкую мышцу без изменения мембранного потенциала Фактически, большинство вазоактивных химических веществ в действительности вызывают изменения мембранного потенциала, поскольку их рецепторы могут быть связаны посредством протеинов G или другим способом с ионными каналами различного типа.
На рис. 8-1 не представлены процессы, удаляющие Са2+ из цитоплазмы клеток гладкой мускулатуры сосудов, хотя они также играют важную роль в создании определенного уровня свободного Са2+ в цитозоле. Как и сердечные клетки (см. рис. 3-7), гладкомышечные клетки активно откачивают кальций в саркоплазматический ретикулум и через сарколемму из клетки. Кальций также выносится из клетки в обмен на натрий.
Механизмы расслабления
Гиперполяризация клеточной мембраны является одним из механизмов, вызывающим расслабление гладкой мускулатуры и расширение сосудов Кроме того, тем не менее, существует, по крайней мере, два основных механизма, посредством которых химические вазодилататоры могут вызвать фармакомеханическую релаксацию гладкой мускулатуры На рис 8-1 рецептор для химического вазоконстриктора был связан с помощью специфического протеина G с фосфолипазой С. Аналогично другие специфические рецепторы могут быть связаны с иными специфическими протеинами G, которые продуцируют отличные от ИТФ вторичные медиаторы ВажнЫм примером является Р2-адренергический рецептор гладкой мышцы, который связан посредством специфического протеина G (Gs) с аденилатциклазой. Аденилатциклаза катализирует превращение АТФ в циклический аденозинмонофосфат (цАМФ). В гладкой мышце цАМФ является вторичным медиатором, который провоцирует снижение концентрации свободного внутриклеточного Са2+, каким-то образом увеличивая скорость выведения кальция из клетки, и его поступления в саркоплазматический ретикулум
Помимо цАМФ, циклический гуанозинмонофосфат (цГМФ) является важным вторичным медиатором, который вызывает расслабление гладкой мускулатуры сосудов посредством не до конца ясных механизмов Образованный из гуанозинтрифосфата под воздействием гуанилатциклазы цГМФ является внутриклеточным энзимом, который может активироваться важным вазодилататором, окисью азота (NO), который продуцируется эндотелиальными клетками Нитроглицерин представляет собой клинически важный вазодилататор, воздействующий на ткани посредством сходного механизма
Сосудистый тонус
Сосудистый тонус — это термин, который обычно используется для характеристики состояния общего сокращения сосуда или сосудистой области Для наших целей понятие «сосудистый тонус» отдела организма может использоваться как показатель «уровня активности» отдельных гладкомышечных клеток данной области.
В действительности эта связьявляется статистическим понятием, так как редко бывает, что все клетки сосуда или все сосуды в определенной области функционируют абсолютно идентично.
Регуляция тонуса артериол
Как описано в главе 7, кровоток через любой орган в значительной степени определяется его сосудистым сопротивлением, которое главным образом зависит от диаметра его артериол. Соответственно, органный кровоток регулируется факторами^ влияющими на тонус гладкой мускулатуры артериол.
Артериолы пребывают в состоянии частичного сужения даже при устранении всех внешних воздействий на них; следовательно, считается, что они обладают определенным базальным тонусом. Наше понимание данного механизма остается туманным, но базальный тонус артериол может быть отражением того факта, что клетки гладкой’ мускулатуры в соответствии с врожденным механизмом активно сопротивляются ра-: стяжению, которое постоянно происходит под действием давления в артериолах. В лю-бом случае базальный тонус устанавливает определенный уровень частичного сужения артериол, от которого внешние воздействия на артериолы «отсчитывают» свои; спазмирующие или дилатирующие эффекты. Эти воздействия можно разделить на три категории: локальные, нервные и гормональные воздействия. ;
Локальные воздействия на артериолы
Локальные метаболические воздействия. Артериолы, регулирующие кровоток через данный орган, сами находятся в тканях данного органа. Таким образом,-артериолы и гладкая мускулатура в их стенках подвергаются действию химического-: состава интерстициальной жидкости органа, который они снабжают. Концентрация.; различных химических веществ в интерстициальной жидкости отражает баланс между метаболической активностью ткани и ее кровоснабжением. Например, уровень кислорода в интерстициальной жидкости всегда падает, если клетки ткани утилизируют кислород быстрее, чем он доставляется в ткани кровотоком. Наоборот, уровень кислорода в интерстициальной жидкости увеличивается, если из крови в ткани поставляется избыточное количество кислорода. Практически во всех сосудистых зонах недостаток кислорода снижает тонус артериол и вызывает расширение сосудов, в то время как высокое содержание кислорода влечет за собой сужение сосудов1. Таким образом-, существует механизм локальной обратной связи, автоматически действующий на уровне артериол, регулируя кровоток в тканях в зависимости от их метаболических потребностей. Если кровоток и доставка кислорода опускаются ниже потребностей ткани в кислороде, то содержание кислорода в тканях вокруг артериол снижается, артериолы расширяются и кровоток через орган увеличивается.
АТФ-чувствительные калиевые каналы клеток гладкой мускулатуры могут представлять один из механизмов, с помощью которых изменения метаболических потребностей тканей приводят к изменениям тонуса артериол. Допустим, например, следующую последовательность событий: (1) при любом варианте недостаточного кровоснабжения тканей в гладкомышечной клетке сосуда возникает снижение уровня АТФ, (2) низкий уровень АТФ приводит к открытию АТФ-зависимых калиевых каналов, (3) открытие любого типа калиевых каналов приводит к гиперполяризации, (4) гиперполяризация приводит к закрытию электроуправляемых Са2+ каналов, (5) уровень свободного Са2+ в цитозоле падает, (6) уровень активации клеток гладкой мускулатуры снижается, (7) сосуды расширяются и (8) кровоток увеличивается для более полного удовлетворения метаболических потребностей тканей.
Многие вещества, помимо кислорода, присутствуют в тканях и могут воздействовать на тонус гладкой мускулатуры сосудов. Например, при увеличении скорости метаболизма скелетной мышцы при физической нагрузке не только снижается уровень кислорода в ткани, но также возрастает содержание СО2, Н+ и К+. Во время физической нагрузки также возрастает и осмолярность мышечной ткани. Все эти изменения химического состава вызывают расширение артериол. Кроме того, при увеличении метаболической активности или снижении содержания кислорода из клеток многих тканей может освобождаться аденозин, который является чрезвычайно активным сосудорасширяющим агентом
В настоящее время мы не знаем, какие из этих (или, возможно, других) изменений содержания химических веществ в тканях наиболее важны с точки зрения локальной метаболической регуляции кровотока. Вероятно, тонус артериол зависит от сочетанного воздействия многих факторов. Кроме того, любой из данных факторов может иметь различную степень значимости в локальной метаболической регуляции кровотока в различных органах
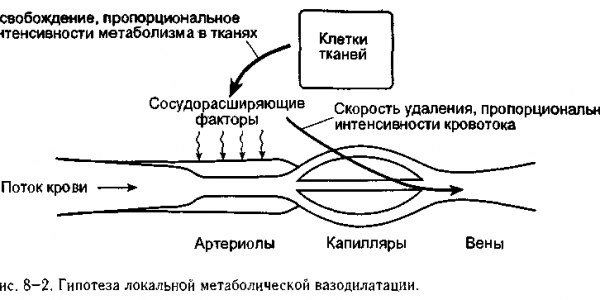
С концептуальной точки зрения наше понимание механизмов локальной метаболической регуляции схематично представлено на рис. 8-2. Сосудорасширяющие агенты поступают в интерстициальное пространство из клеток тканей со скоростью, пропорциональной уровню метаболизма, характерного для данной ткани. Эти сосудорасширяющие агенты удаляются из тканей со скоростью, пропорциональной кровотоку. Если уровень метаболизма в тканях достигает такой величины, что кровоток становится неадекватным, то автоматически возрастает концентрация сосудорасширяющих агентов в интерстиции, что приводит к расширению артериол. Это, конечно, вызывает увеличение кровотока. Процесс продолжается таким образом пока кровоток не возрастает до такой степени, что возникает соответствие между ним и интенсивностью метаболических процессов в ткани, что препятствует дальнейшему накоплению сосудорасширяющих агентов. Эта же система обеспечивает уменьшение кровотока, когда он превышает метаболические потребности тканей, поскольку это приводит к снижению концентрации метаболических факторов вазодилатации в интерстициальной жидкости.
Локальные воздействия эндотелиальных клеток. Клетки эндотелия покрывают всю внутреннюю поверхность сердечно-сосудистой системы. Огромное количество исследований показывает, что кровеносные сосуды реагируют совершенно иначе на определенные воздействия на них при отсутствии эндотелиальной выстилки. Ацетилхолин, например, вызывает вазодилатацию интактного сосуда, но в сосуде, лишенном эндотелиальной выстилки, вызывает вазоконстрикцию. Этот и иные аналогичные результаты привели к пониманию, что эндотелиальные клетки реагируют на различные стимулы посредством продукции локального фактора, который способен снизить тонус вышележащих слоев гладкой мускулатуры. Данное вещество, первоначально названное ЭФР (эндотелиальный фактор релаксации), в настоящее время химически идентифицировано как NO (окись азота). Оно образуется в эндотелиальных клетках из аминокислоты, L-аргинина под действием энзима NO-синтетазы. NO-синтетаза ак-
тивируется при увеличении концентрации внутриклеточного Са2+. NO представляет I собой небольшую жирорастворимую молекулу, которая после образования легко диф-1 фундирует в расположенные рядом клетки гладкой мускулатуры, где она вызывает! релаксацию, предположительно стимулируя продукцию цГМФ. я
Ацетилхолин и некоторые другие вещества (включая брадикинин, вазоактивный! кишечный пептид и субстанцию Р) стимулируют продукцию NO в эндотелиальным клетках, так как их рецепторы на эндотелиальных клетках связаны с рецепторами,Я управляющими Са2+ каналами. Возможно, с физиологической точки зрения более важ-1 но, что определяемое уровнем кровотока напряжение сдвига, воздействуя на эндоте-jj лиальные клетки, стимулирует продукцию ими N0 преимущественно за счет актива»! ции чувствительных к растяжению Са2+ каналов. Такая, зависящая от уровня! кровотока, выработка NO эндотелиальными клетками, возможно, объясняет, почемуа например, физическая нагрузка и увеличение кровотока через мышцы нижней конеч-1 ности могут вызвать расширение бедренной артерии, поставляющей кровь в точках»! которые расположены гораздо выше по течению, чем непосредственно испытывающие! физическое напряжение мышцы. 1
Факторы, которые блокируют продукцию N0 посредством торможения NO-син*! тетазы, вызывают существенное увеличение сосудистого сопротивления в больший^ стве органов в состоянии покоя. Учитывая этот фактор, считается, что эндотелиалы! ные клетки в норме всегда вырабатывают определенное количество NO, что в сочетании! с другими факторами имеет важное значение в создании нормального результирующей! го тонуса артериол в покое во всем организме. 1
Благодаря механизмам, которые в настоящее время не до конца изучены, эндоте-3 лиальные клетки также продуцируют другие расслабляющие факторы (в настоящее| время они носят название «эндотелиальный фактор гиперполяризации») и несколько^ сосудосуживающих факторов, включая эндотелии, очень активный сосудосуживаю- ’ щий пептид. Физиологическая роль данных агентов не до конца установлена. I
Другие локальные химические воздействия. Помимо локальных метаболи-i ческих воздействий на сосудистый тонус, установлены многие специфические хими- i ческие факторы, которые оказывают сосудистые эффекты и поэтому в определенных случаях могут играть важную роль в локальной сосудистой регуляции. Однако в большинстве случаев определенная информация об относительной важности данных веществ в регуляции деятельности сердечно-сосудистой сист^ЭД Отсутствует.
^/^^й^Щ|Й1<ы.предсТ<Й»оТ^обой группу в химическом отношении родственных продуктов И|йЕЛО0ксИгбназиого пути метаболизма арахидоновой кислоты. Определенные простагландины являются мощными вазодилататорами, в то время как другие — мощными вазоконстрикторами. Несмотря на потенциальные вазоактивные воздействия простагландинов и тот факт, что большинство тканей (включая эндотелиальные клетки и клетки сосудистой гладкой мускулатуры) способны синтезировать простагландины, не было убедительно показано, что простагландины играют решающую роль в нормальной регуляции деятельности сосудов. Однако ясно, что сосудорасширяющие простагландины принимают участие в воспалительной реакции. Соответственно, ингибиторы синтеза простагландинов, такие как аспирин, являются эффективными противовоспалительными лекарствами. Простагландины, продуцируемые тромбоцитами и эндотелиальными клетками, играют важную роль в гемостатической вазоконстрикции (прекращающей кровоток, останавливающей кровотечение) и агрегации тромбоцитов при повреждении сосудов Следовательно, аспирин часто используется для уменьшения тромбообразования — особенно у больных с потенциальными нарушениями коронарного кровотока. Метаболиты арахидоновой кислоты, образующиеся посредством липооксигеназной системы (например, лейкотриены), также обладают вазоактивными свойствами и при определенных условиях могут влиять на кровоток.
Гистамин синтезируется и запасается в большой концентрации в секреторных гранулах тканевых тучных клеток и циркулирующих базофилов. При освобождении из гранул гистамин вызывает дилатацию артериол и увеличение сосудистой проницаемости, что ведет к накоплению жидкости и образованию локальных отеков в тканях Гистамин увеличивает проницаемость сосудов, разрыхляя соединение между соседними эндотелиальными клетками, выстилающими сосудистую систему. Освобождение гистамина классически ассоциируется с реакциями антиген—антитело при различных аллергических и иммунных реакциях. Многие лекарственные, химические и физические воздействия, повреждающие ткани, также вызывают освобождение гистамина Гистамин способен стимулировать чувствительные нервные окончания, что вызывает зуд и болевые ощущения. Важность участия гистамина во многих патологических ситуациях не вызывает сомнения, однако нет убедительных данных об участии гистамина в нормальной регуляции деятельности сердечно-сосудистой системы.
Брадикинин и каллидин являются полипептидами, активность молекул которых как вазодилататоров почти в 10 раз превышает активность молекулы гистамина. Эти кинины также повышают проницаемость капилляров путем открытия соединений между эндотелиальными клетками. Они образуются из определенных глобулинов плазмы под воздействием фермента калликреина и в последующем быстро распадаются до неактивных фрагментов под действием различных тканевых киназ Считается, что подобно гистамину брадикинин и каллидин участвуют в сосудистых реакциях при повреждении тканей и в иммунных реакциях. Кинины стимулируют ноцицептивные нервы и поэтому могут участвовать в болевой реакции, связанной с травмой ткани.
Трансмуральное давление. В главе 7 мы обсуждали пассивные эластические механические свойства артерий и вен и каким образом изменения трансмурального давления оказывают воздействие на величину их диаметра. Влияние трансмурального давления на диаметр артериол более сложное, так как артериолы реагируют как пассивно, так и активно на изменение трансмурального давления. Например, внезапное увеличение внутреннего давления в артериоле приводит (1) сперва к начальному небольшому пассивному растяжению (небольшому, поскольку артериолы обладают от-носительио толстой и мышечной стенкой) и (3) затем активному сжато, которое за несколько секунд может полностью нейтрализовать первоначальное растяжение Внезапное уменьшение трансмурального давления вызовет прямо противоположную реакцию, т е мгновенное пассивное уменьшение диаметра, вслед за чем быстро следует снижение активного тонуса, что приведет к возвращению диаметра артериол почти к той же величине, что отмечалась перед изменением давления Активная фаза данного процесса называется гипогенной реакцией, поскольку складывается впечатление, что она возникает непосредственно в самой гладкой мышце Механизм миогенной реакции остается не до конца ясным, но чувствительные к растяжению ионные каналы в клетках гладкой мускулатуры артериол являются наиболее вероятными звеньями, участвующими в данном процессе
Во всех артериолах в норме существует некоторое давление растяжения, на которое они, возможно, активно реагируют Как мы уже отмечали, представляется возможным, что миогенный механизм является фундаментально важным фактором создания повсеместного базального тонуса артериол Также, по очевидным причинам и как вскоре будет обсуждено, миогенная реакция считается компонентом сосудистой реакции на любое расстрой ство в деятельности сердечно-сосудистой системы, при котором происходит изменение трасмурального давления в артериолах
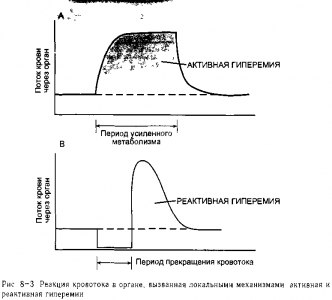
Изменения кровотока, обусловленные локальными механизмами. В органах, где интенсивность метаболических реакций существенно колеблется, таких как' скелетная и сердечная мышца, кровоток теснейшим образом реагирует на интенсив-) ность метаболизма в тканях Например, кровоток в скелетной мышце увеличивается в1 течение нескольких секунд после начала физической нагрузки на мышцу и возвраща-: ется к исходным величинам сразу после того, как физическая нагрузка прекращается. t Данный феномен, который проиллюстрирован на рис 8-3, А, называется нагрузочной, или активной, гиперемией (термин гиперемия означает усиленный кровоток).1? Должно быть ясно, каким образом активная гиперемия могла возникнуть в результате* работы механизма обратной локальной метаболической сосудорасширяющей связи гладкой мускулатуры артериол
Реактивная, или постокклюзионная, гиперемия представляет собой более высокий, чем в норме, кровоток, временно возникающий после устранения любого препятствия, которое привело к снижению кровотока (рис 8-3, В) Например, в течение некоторого времени после снятия жгута с конечности, кровоток в ней выше нормы. В процесс возникновения реактивной гиперемии могут быть вовлечены как локальные метаболические, так и миогенные механизмы Выраженность и длительность реактивной гиперемии зависит от длительности и степени непроходимости сосуда (окклюзии), а также от метаболической активности ткани Эти данные могут быть лучше объяснены накоплением в интерстициальной жидкости метаболитов, обладающих сосудорасширяющим эффектом, во время периода ограничения кровотока В то же время после артериальной окклюзии, длящейся всего 1 -2 с, может возникнуть неожиданно большое увеличение кровотока Лучше всего это может быть объяснено миогенной реакцией дилатации на уменьшение внутрисосудистого давления и снижение растяжения стенки артериолы, что отмечается во время окклюзии
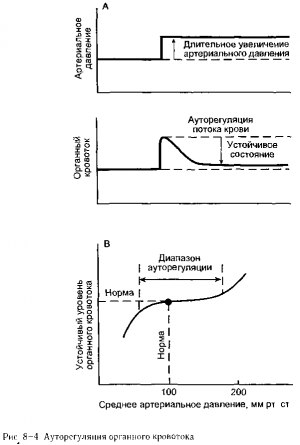
За исключением случаев, когда развивается активная и реактивная гиперемия, почти во всех органах отмечается тенденция к поддержанию постоянного уровня кровотока, несмотря на изменения артериального давления, т е они (органы) обладают ауторегуляцией кровотока Как показано на рис 8-4, А, резкое увеличение артериального давления обычно сопровождается первоначальным интенсивным возрастанием органного кровотока, который затем постепенно возвращается к норме, несмотря
на сохраняющийся подъем артериального давления Первоначальное увеличение кровотока на фоне повышения артериального давления можно предсказать, исходя из основного уравнения гидродинамики (Q=AP/R) Последующее возвращение кровотока к нормальному уровню вызвано постепенным увеличением величины активного тонуса артериол и сосудистого сопротивления кровотоку
В конце концов, новое устойчивое состояние достигается лишь при незначитель ном повышении кровотока, так как увеличенное движущее давление компенсируется более высоким чем в норме, сосудистым сопротивлением Как и в случае феномена реактивной гиперемии, ауторегуляция кровотока может осуществляться как с помощью механизмов локальной метаболической обратной связи, так и за счет миогенных механизмов Сужение артериол, ответственное за реакцию ауторегуляции, показан ное на рис 8-4, А, например, может быть частично обусловлено (1) «вымыванием» сосудорасширяющих метаболитов из интерстициального пространства в результате первоначального усиления кровотока и (2) миогенным увеличением тонуса артериол, вызванного увеличением сил растяжения, воздействующих на сосудистую стенку при повышенном давлении
Кроме того существует гипотеза тканевого давления, объясняющая способность кровотока к ауторегуляции, в соответствии с которой считается, что резкое увеличение артериального давления влечет за собой транскапиллярную фильтрацию жидкости и тем самым приводит к постепенному увеличению объема и давления ин-
терстициальнои жидкости Преимущественно увеличение экстравазального давления должно вызывать уменьшение диаметра сосудов в результате их простого сжатия Такой механизм может быть особенно важен в таких органах, как почки и головной мозг объемы которых стеснены внешними анатомическими структурами
Хотя на рис 8-4, А это не представлено, механизмы ауторегуляциии действуют в противоположном направлении в ответ на снижение артериального давления ниже нормы Одно из основных важных следствии деятельности местных механизмов ауторегуляции заключается в том, что кровоток в состоянии покоя во многих органах обладает тенденцией оставаться близким к норме при широком диапазоне значении артериального давления Это показано на рис 8-4, В Как мы обсудим позже, автономная способность определенных органов поддерживать адекватный кровоток, несмотряйа более низкое, чем в норме, артериальное давление, является фактором чрезвычайной важности в таких ситуациях, как шок, обусловленный кровопотерей
Нервная регуляция тонуса артериол
Симпатические сосудосуживающие волокна. Эти нервные волокна иннервируют артериолы во всех системных органах и являются наиболее важным фактором рефлекторной регуляции сосудов Эти нервы выделяют норадреналин из своих окончаний в количествах, главным образом, пропорциональных их электрической активности1 2 3 Норадреналин вызывает увеличение тонуса артериол после соединения с а-адренергическими рецепторами гладкомышечных клеток Считается, что норадреналин увеличивает сосудистый тонус преимущественно за счет фармакомеханичес-ких процессов Этот механизм включает связь протеина G а-адренергических рецепторов с фосфолипазой С и последующее освобождение Са2+ из внутриклеточных депо под воздействием вторичного медиатора ИТФ, как это было показано в фармакомеха-нической части рис 8-1
Симпатические сосудосуживающие нервы в норме обладают постоянной, или тонической «тлеющей», активностью. Эта тоническая активность симпатических сосудосуживающих нервов приводит к тому, что тонус сократительных мышц артериол в норме существенно больше, чем их базальный тонус Этот дополнительный компонент сосудистого тонуса называется нейрогенным тонусом Когда интенсивность импульсаций симпатических сосудосуживающих нервов увеличивается выше нормы, артериолы спазмируются, что влечет за собой снижение органного кровотока по сравнению с нормой Наоборот, вазодилатация и увеличение органного кровотока вызывается симпатическими сосудосуживающими нервами, если уровень их нормальной тонической активности снижен Таким образом, органный кровоток может быть снижен или увеличен по сравнению с нормой в результате изменения импульсации симпатических сосудосуживающих волокон
Другие нервные воздействия. Кровеносные сосуды, как правило, не получают иннервации из парасимпатического отдела вегетативной нервно й системы В то же время парасимпатические сосудорасширяющие нервы, которые выделяют ацетилхолин, имеются в сосудах мозга и сердца, но их воздействие на тонус артериол данных органов является несущественным Парасимпатические сосудорасширяющие нервы также находятся в сосудах слюнных желез, поджелудочной железы, слизистой оболочки желудка и наружных половых органов В последних они ответственны за расширение приносящих кровь сосудов, регулирующих эрекцию
Гормональная регуляция тонуса артериол
В обычных условиях воздействие гормонов на сосуды считав гея несущественным = по сравнению с локальными метаболическими и нервными воздействиями. В то же i время следует отметить, что наше понимание того, как сердечно-сосудистая система | функционирует во многих ситуациях, остается неполным. Таким образом, обсуждае-1 мые ниже гормоны могут играть более важную роль в регуляции деятельности сердец-1 но-сосудистой системы, чем мы думаем. з
Циркулирующие катехоламины. При активации симпатической нервной! системы надпочечники выделяют в кровоток катехоламины — адреналин и норад-Л реналин. В нормальных условиях уровень в крови данных агентов, возможно, нм столь высок, чтобы существенно повлиять на деятельность сердечно-сосудистоИ системы. Однако циркулирующие в крови катехоламины могут оказывать воздей-З ствие на сердечно-сосудистую систему в условиях (таких как очень интенсивная! физическая нагрузка или геморрагический шок) высокой активации симпатичеЛ ской нервной системы. В целом воздействие на сердечно-сосудистую систему высоЛ кого уровня циркулирующих катехоламинов аналогично непосредственному возЛ действию активирования симпатического отдела нервной системы, которое мы ужя обсуждали. Как адреналин, так и норадреналин могут активировать [З-адренерпД ческие рецепторы сердца, увеличивая частоту сердечных сокращений и сократив тельную способность миокарда, а также могут активировать а-рецепторы сосудовя вызывая их сужение. Помимо а-рецепторов, которые опосредуют вазоконстрим цию, в артериолах многих органов также имеются [3-адренергические рецепторыж которые опосредуют вазодилатацию4. [3-Рецепторы сосудов более чувствительны м адреналину, чем а-рецепторы сосудов, так что низкий уровень адреналина в кровя может вызвать вазодилатацию, в то время как высокий его уровень вызывает опоев редованную а-рецепторами вазоконстрикцию. Сосудистые [3-рецепторы не имею® иннервации и поэтому не активируются в результате освобождения норадреналинЯ из окончаний симпатических сосудосуживающих нервов. Функциональное значеЛ ние данных [3-рецепторов сосудов не ясно, поскольку освобождение адреналина изй надпочечников происходит при увеличении активности симпатического отделяя когда артериолы претерпевают одновременную прямую нейрогенную вазоконст! рикцию. 1
Вазопрессин. Этот полипептидный гормон, также известный под названием аня тидиуретический гормон (АДГ), играет важную роль в гомеостазе внеклеточной жид-1 кости и поступает в кровоток из задней доли гипофиза в ответ на уменьшение внекле4 точного объема и (или) повышение осмолярности внеклеточной жидкости. Вазопрессин] воздействует на собирательные трубки почек, уменьшая экскрецию воды почкамИЛ Его функциональная роль в регуляции жидк остного состава организма оказывает н&| которые очень важные опосредованные воздействия на сердечно-сосудистую систему! что будет детально обсуждено в главе 10. Вазопрессин в то же время является актив-1 ным агентом, суживающим артериолы Хотя представляется, что его роль в регуляции нормального сосудистого тонуса не слишком велика, непосредственное сосудосужи! вающее действие необычно высокого уровня вазопрессина может быть важным фактор ром в реакции на определенные нарушения, такие как выраженная потеря крови при кровотечении. ]
Ангиот®ЙЙ1ЖЭйгио?ёйз'иН И является циркулирующим полипептидом, который регулирует высвобождение альдостерона из коры надпочечников, являясь составной частью системы, регулирующей содержание натрия в организме. Эта система, более детально обсуждаемая в главе 10, имеет очень большое значение для регуляции объема крови. Ангиотензин II является также очень сильным сосудосуживающим агентом. Хотя его тоже не рассматривают как фактор регуляции тонуса артериол в нормальных условиях, но непосредственное сосудосуживающее влияние ангиотензина II считается важным компонентом общей реакции сердечно-сосудистой системы на выраженную кровопотерю. Также есть убедительные данные о том, что непосредственное воздействие ангиотензина II на сосуды может иметь значение во внутрипочечных механизмах регуляции деятельности почек. Кроме того, ангиотензин II может частично обусловливать патологическую вазоконстрикцию, которая сопровождает многие формы артериальной гипертензии. Опять же следует отметить, что наши знания о многих патологических состояниях — в том числе об артериальной гипертензии — являются неполными. При этих состояниях могут включаться такие факторы, о существовании которых мы до сих пор пока не знаем.
Регуляция венозного тонуса
Перед тем как обсудить детали регуляции венозного тонуса, напомним, что венулы и вены играют совершенно иную роль в сердечно-сосудистой системе, чем артериолы. Артериолы являются входными клапанами, которые регулируют интенсивность питательного кровотока через органы и отдельные участки их. Соответственно, артериолы обычно находятся под сильным влиянием текущих локальных метаболических потребностей зоны, где они расположены, в то время как вены не испытывают таких воздействий. В то же время вены в своей совокупности регулируют распределение имеющегося объема крови между периферическим и центральным венозными пулами. Напомним, что центральный объем крови (и следовательно, давление) оказывает существенное воздействие на ударный объем и минутный объем сердца. Соответственно, при рассуждении о процессах в периферических венах следует, прежде всего, иметь в виду их влияние на центральное венозное давление и минутный объем.
В стенках вен находится гладкая мускулатура, которая испытывает воздействие многих факторов, которые оказывают влияние и на гладкую мускулатуру артериол. Сужение вен (веноконстрикция) в значительной степени определяется активацией их симпатической иннервации. Как и в артериолах, эти симпатические нервы выделяют норадреналин, который взаимодействует с а-рецепторами, что приводит к увеличению венозного тонуса и уменьшению диаметра сосуда. Однако между венами и артериолами есть несколько важных функциональных отличий. По сравнению с артериолами вены в норме обладают незначительным базальным тонусом. Поэтому в норме вены находятся в расширенном состоянии. Одним из важных следствий отсутствия базального сосудистого тонуса вен является то, что метаболиты с сосудорасширяющим эффектом, которые могут накапливаться в тканях, оказывают слабое влияние на вены.
Из-за того, что у них тонкая стенка, вены гораздо в большей степени чувствительны к физическим воздействиям, чем артериолы. Существенное влияние внутреннего венозного давления на диаметр вен обсуждался в главе 7 и это хорошо видно по накоплению крови в венах нижних конечностей при длительном стоянии (как это будет обсуждено в главе 11). Напомним, что изменения сосудистого сопротивления артери-
ол (см. рис. 7-6) и, вследствие этого, тонус артериолоказывает непрямое влияние на диаметр вен Сужение артериол имеет тенденцию понижать венозное давление и тем самым уменьшать диаметр вен Расширение артериол оказывает противоположное действие надиаметр вен
Часто внешние сжимающие силы являются важным фактором, влияющим на венозный объем Это утверждение особенно справедливо для вен скелетной мускулатуры Во время сокращения скелетной мускулатуры в ней развивается очень высокое давление, что приводит к спадению вен Поскольку в венах и венулах располагаются однонаправленные клапаны, то кровь во время сокращения скелетной мускулатуры перемещается в венах только в одном направлении к правому сердцу Фактически ритмические сокращения скелетной мускулатуры могут оказать выраженный насосный эффект, что часто называется насосом скелетной мускулатуры, в результате деятельности которого облегчается возврат крови к сердцу при физической нагрузке
Обзор основных механизмов регуляции тонуса сосудов
Сосуды подвергаются разнообразным воздействиям, и определенные влияния име-1 ют особенное значение для отдельных органов Однако определенные общие факторы] преобладают в регуляции тонуса периферических сосудов, если рассмотреть этот про-] цесс с точки зрения деятельности сердечно-сосудистой системы в целом, эти факторьц представлены на рис 8-5 1
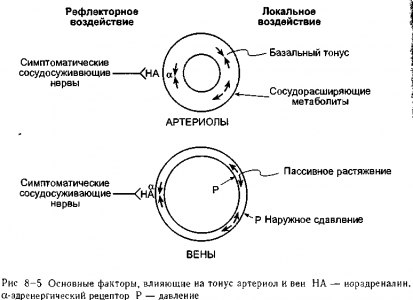
факторы и симпатические сосудосуживающие нервы, воздействующие через а-рецеп-торы, являются основными факторами, регулирующими тонус артериол и, следовательно, кровоток через периферические органы Симпатические сосудосуживающие нервы, внутрисосудистое давление и внешние сдавливающие силы являются наиболее значимыми воздействиями на диаметр вен и, соответственно, на объем крови в периферических органах
Регуляция тонуса сосудов в отдельных органах
Как станет очевидным из последующих разделов данной главы, конкретные детали регуляции тонуса сосудов отличаются в различных органах В то же время, с точки зрения регуляции кровотока, большинство органов может быть расположено в ряду, где, с одной стороны, будут почти полностью доминировать локальные метаболические механизмы а с другой стороны, будут полностью преобладать симпатические нервы Важные общие функциональные отличия способов регуляции кровотока между органами на полюсах данного спектра представлены на рис 8-6
В таких органах, как головной мозг, сердечная и скелетная мышцы нормальный органный кровоток существенно ниже максимального, поскольку в норме тонус органных артериол в покое высокий, как это показано на рис 8-6, А Обычно нормальный кровоток не намного больше необходимого для удовлетворения нормальных метаболических потребностей тканей Как показано на рис 8-6, А, изменения активности симпатических сосудосуживающих волокон оказывают очень незначительное воздействие на кровоток в данных органах по сравнению с воздействием, обусловленным изменением их метаболической активности Увеличение активности симпатических сосудосуживающих волокон не способно снизить кровоток за счет вазоконстрикции, так как это воздействие ведет к повышению содержания тканевых сосудорасширяющих метаболитов которые оказывают противоположный эффект и ограничивают уменьшения кровотока Уменьшение активности симпатических сосудосуживающих волокон, напротив, может вызвать только умеренное увеличение кровотока в данных органах, так как базальный тонус артериол в них высокий Однако увеличение интенсивности метаболических процессов в тканях и образование сосудорасширяющих ве ществ при метаболизме может вызвать значительное увеличение кровотока в результате снижения нормального высокого тонуса артериол
Значительно отличная ситуация наблюдается в почках коже и органах брюшной полости, как показано на рис 8-6, В Нормальный кровоток в данных органах относительно высок и обычно существенно превышает минимальные метаболические потреб ности тканей этих органов, следовательно, концентрация в их тканях сосудорасширяющих метаболитов очень низкая Как показано на рис 8-6, В, увеличение активности симпатических сосудосуживающих волокон влечет за собой существенное уменьшение кровотока в данных органах Частично это происходит вследствие того, что нор мальный тонус артериол существенно ниже, чем максимально возможный, а вследствие того, что симпатическая вазоконстрикция не полностью уравновешивается локальной метаболической вазодилатацией в данных органах Обычно, даже сниженный в результате симпатической вазоконстрикции кровоток, достаточен для обеспечения основных метаболических потребностей тканей
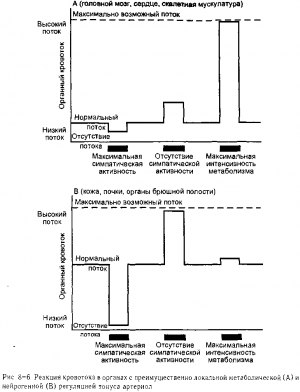
В то же время такое снижение кровотока может сократить какую-либо функцию рассматриваемого органа по поддержанию состава крови, и поэтому снижение кровотока может переноситься временно, но не может продолжаться неопределенно долго. Как показано на рис 8-6, В, кровоток в данных органах увеличивается почти до максимума при отсутствии воздействия симпатических нервов. Отсюда можно сделать вывод, что артериолы в данных органах обладают незначительным базальным тонусом. Однако повышенйеметаболачеСкой активности данных органов оказывает очень незначительное воздействие на кровоток» поскольку нормальный высокий кровоток предотвращает накопление сосудорасширяющих метаболитов в концентрациях, способных изменить тонус артериол. Органы, в которых кровоток регулируется преимущественно симпатическими нервами, в значительной степени участвуют в рефлекторных реакциях сердечно-сосудистой системы, что будет обсуждено в главах 10 и 11.
Коронарный кровоток
Главные правая и левая коронарные артерии, которые снабжают ткани сердца, являются первыми сосудами, отходящими от аорты. Таким образом, силой, определяющей кровоток в миокарде, является системное артериальное давление, каки в других системных органах. Большая часть крови, протекающей через ткани миокарда, возвращается в правое предсердие через большую сердечную вену, которая называется коронарным синусом.
Локальная метаболическая регуляция. Как уже указывалось, коронарный кровоток, прежде всего, регулируется локальными метаболическими механизмами и таким образом быстро и точно реагирует на изменения в потреблении кислорода миокардом. У человека в покое ткани миокарда потребляют от 70 до 75% кислорода из крови, протекающей через них. В крови коронарного синуса в норме содержание кислорода ниже, чем в крови любого другого участка сердечно-сосудистой системы. Извлечение кислорода миокардом из крови не может существенно возрасти по сравнению с состоянием покоя.
Следовательно, увеличение потребления кислорода миокардом должно сопровождаться соответственным возрастанием коронарного кровотока. В действительности коронарный кровоток в норме соответствует потреблению кислорода миокардом настолько точно, что уровень кислорода в крови коронарного синуса практически не меняется, несмотря на изменения потребления кислорода тканями миокарда
Какой из метаболических сосудорасширяющих факторов играет доминирующую роль в регуляции тонуса коронарных артериол, в настоящее время не известно. Многие исследователи считают, что аденозин, освобождаемой из миокардиальных клеток при недостатке кислорода, может оказывать важное воздействие в качестве локального коронарного метаболического вазодилататора. Независимо от мелких деталей потребление кислорода миокардом обладает наиболее важным влиянием на коронарный кровоток.
Систолическое сжатие. Во время сокращения сердечной мышцы в ткани миокарда возникают значительные силы и (или) давление Эти интрамиокардиальные силы оказывают внешнее давление на коронарные сосуды и вызывают их спадение во время систолы Вследствие этого систолического сжатия и связанного с ним спадения коронарных сосудов сопротивление коронарных сосудов во время систолы существенно возрастает В результате, по крайней мере, в большей части миокарда левого желудочка коронарный кровоток во время систолы меньше, чем во время диастолы, несмотря на то, что системное артериальное давление (т е коронарное перфузионное давление) является самым высоким во время систолы Сказанное иллюстрируется графиком кровотока в левой коронарной артерии на рис. 8-7 Систолическое сжатие оказывает гораздо меньшее влияние на кровоток в миокарде правого желудочка, что видно на графике кровотока в правой коронарной артерии на рис 8-7 Так происходит потому, что максимальное систолическое внутрижелудочковое давление существенно ниже в правом сердце, чем в левом, и силы систолического сжатия в стенке правого желудочка, соответственно, ниже, чем в стенке левого желудочка.
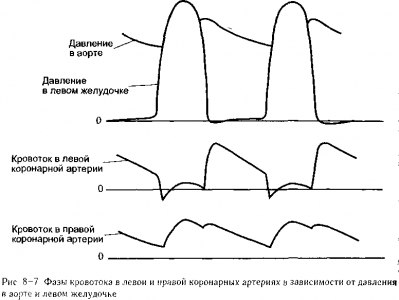
Силы систолического сжатия, воздействующие на коронарные сосуды, выше в эндокардиальных (внутренних) слоях стенки левого желудочка, чем в эпикардиальных слоях3 Таким образом, систолическое сжатие снижает кровоток в эндокардиальных слоях левого желудочка в большей степени, чем в эпикардиальных слоях В норме эндокардиальная зона миокарда может компенсировать недостаточный кровоток во время систолы за счет усиленного кровотока во время диастолы Однако когда коронарный кровоток ограничен — например, при патологии коронарных сосудов и их стенозе — эндокардиальные слои левого желудочка первыми испытывает трудности с обеспечением уровня кровотока, соответствующего метаболическим потребностям тканей Инфаркты миокарда (участки ткани, погибшей в результате дефицита кровотока) возникают чаще всего в эндокардиальных слоях левого желудочка
Нервная регуляция коронарного кровотока. Коронарные артериолы густо иннервированы симпатическими сосудосуживающими волокнами, однако при повышении активности симпатической нервной системы, коронарные артерии в норме скорее расширяются, чем суживаются Это происходит потому, что увеличение симпатического тонуса увеличивает потребление кислорода миокардом вследствие возрастания частоты и силы сердечных сокращений Увеличение местных метаболических сосудорасширяющих влияний, очевидно, превышает конкурирующее сосудосуживающее воздействие, обусловленное увеличением активности симпатических сосудосуживающих нервных окончаний коронарных артериол
-i tЭксперимёйтйЙВНО’тюХазямсЬ-что данное увеличение активности кардиальных симпатических нервов вызывает большее увеличение коронарного кровотока при уст ранении непосредственного сосудосуживающего действия симпатических нервов на коронарные сосуды с помощью а-адреноблокаторов В то же время представляется, что симпатические сосудосуживающие нервы не оказывают влияния на коронарный кровоток, достаточного для изменения механической деятельности нормально работающего сердца Вопрос о том, являются ли данные коронарные сосудосуживающие волокна функционально значимым фактором при определенных патологических условиях, остается открытым
Как уже указывалось ранее, коронарные артериолы также получают иннервацию парасимпатическими сосудорасширяющими волокнами В то же время их роль в регуляции нормального коронарного кровотока считается несущественной
Кровоток в скелетной мускулатуре
В целом масса скелетной мускулатуры составляет 40-45% от общей массы тела — больше, чем любого иного, отдельно взятого органа тела Даже в состоянии покоя около 15% минутного объема крови направляется к скелетной мускулатуре, а во время интенсивной физической нагрузки скелетные мышцы могут получать до 70% от минутного объема крови Таким образом, кровоток в скелетной мускулатуре является важным фактором в общей гемодинамике
Вследствие высокого уровня автономного тонуса сосудистого сопротивления в скелетной мускулатуре в покое, кровоток на 1 г ткани достаточно низок по сравнению с соответствующими показателями других органов, например, почек В то же время кровоток скелетной мускулатуры в покое несколько превышает уровень, необходимый для покрытия ее метаболических потребностей В норме скелетная мускулатура в покое потребляет только 25-30% кислорода, доставляемого к ней артериаль ной кровью Изменения активности симпатических сосудосуживающих волокон изменяют кровоток в мышцах в покое
Например, при максимальной симпатической импульсации кровоток мускулатуры в покое может снизиться до 1 / от его нормального размера и, соответственно, наоборот, если полностью устранить нейрогенный сосудистый тонус, то кровоток в мускулатуре в покое может увеличиться вдвое Такое увеличение кровотока не велико по сравнению с 20 кратным возрастанием, которое происходит в скелетной мускулатуре при физическом нагрузке Темне менее, из-за значительной массы ткани изменения сосудистого сопротивления скелетной мускулатуры в покое в результате изменения симпатической активности оказывают большое влияние на рефлекторную регуляцию артериального давления в целом
Особенно важным свойством скелетной мышцы является очень широкий диапазон метаболической активности Во время интенсивной физической нагрузки скорость потребления кислорода и экстракция его скелетной мышцей могут достигать значительных величин характерных для миокарда Во многих отношениях факторы, регулирующие кровоток в скелетной мышце при нагрузке, сходны с теми, которые регулируют коронарный кровоток Локальная метаболическая регуляция тонуса артериол в мышце при физической нагрузке является весьма жесткой и потребление кислорода мышцей является наиболее важным фактором, определяющим кровоток в скелетной мышце при нагрузке
Как будет обсуждено далее в главе 11, реакция сердечно сосудистой системы на физическую работу мышцы включает общее повышение симпатической активности Данное увеличение активности симпатических нервов вызывает существенно мень-
шее относительное (в процентном отношении) снижение интенсивности кровотока в I работающей мышце по сравнению с мышцей в покое. Таким образом, считается, что | физическая нагрузка, так или иначе, тормозит влияние симпатических нервов на то- 1 нус артериол в скелетной мышце. Частично это объясняется наличием выраженных I локальных метаболических сосудорасширяющих влияний на артериолы работающих а мышц. Также локальное увеличение концентрации Н+, К+, осмолярности и аденозина 1 может снизить высвобождение норадреналина из окончаний симпатических нервов во 1 время физической нагрузки. Однако остается фактом, что общее увеличение симпати- а ческой активности, обычно происходящее при физической нагрузке, до определенной Л степени снижает степень локальной метаболической вазодилатации в работающих мыш- 1 цах. Похоже, что это не оказывает неблагоприятного воздействия на работу мышцы 1 при субмаксимальных усилиях, но максимальный мышечный кровоток, интенсивность Я поглощения кислорода и работа мышцы уменьшаются в результате активации симпа- я тической иннервации. 1
Каки в сердце, сокращение мышцы создает в тканях мощные компрессионные силы, Я которые могут вызвать сжатие сосудов и уменьшить кровоток. Сильное, постоянное I (тетаническое) сокращение скелетной мышцы может фактически прекратить кровоток Я в ней. Около 10% от общего объема крови в норме содержится в венах скелетной муску- Я латуры, и во время ритмических сокращений последних «мышечный насос» эффективно 1 перемещает кровь из вен скелетной мускулатуры. Кровь, вытесненная из скелетной мус- Я кулатуры в центральный венозный пул, является для всего организма важным гемодина- Я мическим фактором при интенсивной физической нагрузке. Я
Вены скелетной мускулатуры иннервированы симпатическими сосудосуживаю- Д щими волокнами достаточно редко, и весьма небольшой объем крови, который может 1 быть мобилизован из скелетной мускулатуры при активации симпатических нервов, я вероятно, не играет существенной роли в гемодинамике организма в целом. Это резко я отличается от значительного перемещения крови из мышцы при физической нагрузке Ц в результате действия механизма мышечного насоса.
Мозговой кровоток
Адекватный мозговой кровоток представляет собой фактор особой важности для 1 выживания организма, поскольку очень быстро после прекращения кровотока в мозге | наступает потеря сознания. Одним из общих правил функционирования сердечно-со- 1 судистой системы является то, что при любых условиях она стремиться сохранить | адекватный кровоток в головном мозге
В мозге в целом существует почти постоянный уровень метаболической активно- 1 сти, который при пересчете на 1 г вещества почти столь же высок, как и в ткани мио-карда Представляется, что церебральный кровоток регулируется почти полностью J локальными механизмами Кровоток мозга подвергается жесткой ауторегуляции, и на ; него мало влияют колебания артериального давления, пока оно не падает ниже 60 мм . рт. ст. Когда артериальное давление снижается ниже 60 мм рт. ст., мозговой кровоток пропорционально уменьшается. В настоящее время остается неизвестным, участвуют ли в ауторегуляции мозгового кровотока метаболические механизмы или миогенные механизмы или оба эти варианта.
Предположительно, поскольку общая средняя метаболическая активность тканей мозга колеблется незначительно, общий мозговой кровоток является удивительно постоянным почти в любых условиях. Активность конкретаЫХотделов мозга в то же время постоянно изменяется. Вследствие этого кровото|^н^вДеленных отделах не является пЩЙВйМя чутИВГреагирует на локальную активность нейронов. М еха-низмы, осуществляющие столь строгую локальную регуляцию церебрального кровотока, до сих пор в деталях не установлены, но в них, скорее всего, участвуют такие факторы, как концентрация Н+, К+, О2 и аденозина.
Церебральный кровоток увеличивается всегда, когда парциальное давление двуокиси углерода (Рсо2) в артериальной крови превышает норму. Наоборот, мозговой кровоток снижается, если Рсо2 в артериальной крови уменьшается ниже нормы. Представляется, что артериолы мозга реагируют не на изменения Рсо2, а на изменения внеклеточной концентрации Н+ (т.е. pH), вызванные изменениями Рсо2. Артериолы мозга также расширяются, если парциальное давление кислорода (Ро2) в артериальной крови падает существенно ниже нормальных значений. Более высокий уровень, чем в норме Ро2, например, в результате ингаляции кислорода, приводит только к небольшому снижению церебрального кровотока.
Хотя церебральные сосуды получают каксимпатические сосудосуживающие, так и парасимпатические сосудорасширяющие волокна, но в норме мозговой кровоток меняется очень слабо под влиянием этих факторов. Реакция симпатических сосудосуживающих нервов в тоже время считается важным защитным механизмом, предохраняющим мозговые сосуды от избыточного пассивного растяжения при внезапном, значительном увеличении артериального давления.
Уникальность мозговых капилляров заключается в том, что они гораздо в меньшей степени проницаемы, чем в других органах, что существенно ограничивает транскапиллярное перемещение полярных частиц. Ограничение диффузии и другие специфические метаболические механизмы, связанные с эндотелиальными клетками мозговых капилляров, создают то, что называется гематоэнцефалическим барьером^ . Благодаря гематоэнцефалическому барьеру, внеклеточное пространство мозга представляет собой жидкостное пространство, химический состав которого регулируется независимо от состава плазмы и остальной внеклеточной жидкости организма Внеклеточное пространство мозга содержит как интерстициальную жидкость, так и цереброспинальную жидкость (ЦСЖ), которая окружает головной и спинной мозг и заполняет мозговые желудочки. ЦСЖ образуется из плазмы в результате селективной секреции (а не простой фильтрации) специализированными тканями, сосудистыми сплетениями, расположенными в желудочках. Этот процесс регулирует химический состав ЦСЖ. Интерстициальная жидкость головного мозга получает химический состав ЦСЖ в процессе обмена путем свободной диффузии.
Гематоэнцефалический барьер защищает клетки мозга от нарушений ионного равновесия в плазме. Также с помощью ограничения и (или) метаболизма в эндотелиальных клетках он предотвращает воздействие циркулирующих гормонов (и многих лекарств) на паренхиматозные клетки мозга и клетки гладкой мускулатуры мозговых сосудов
Кровоток в органах брюшной полости
Значительное число органов брюшной полости, в том числе органы пищеварительного тракта, селезенка, поджелудочная железа и печень, в целом, получают кровоснабжение за счет чревного кровотока. Чревный кровоток поступает к данным
органам по многим артериям, но в конечном итоге данная кровь протекает через печень и возвращается в нижнюю полую вену через печеночные вены
Органы брюшной полости получают около 25% от всего минутного объема крови в покое и, кроме того, содержат более 20% от циркулирующего оОъема крови Таким образом, кровоток или объем крови в данном сосудистом регионе оказывает чрезвычайно важное воздействие на деятельность сердечно-сосудистиой системы в целом
Между отдельными органами брюшной полости, и даже их отделами, существуют значительные функциональные различия Кровоток необходим для осуществления процессов всасывания и секреции, а также процессов мышечного сокращения в органах желудочно-кишечного тракта Механизмы регуляции деятельности сосудов органов брюшной полости не до конца изучены, но известно, что они чрезвычайно разнообразны Тем не менее, так как большинство органов брюшной полости участвует в процессе пищеварения и всасывания из пищеварительного тракта, после приема пищи чревный кровоток возрастает После обильного приема пищи кровоток в органах брюшной полости может увеличиться на 30-100%, но в отдельных органах данной группы процентное увеличение кровотока может достигать еще больших величин в различные моменты времени, поскольку они последовательно включаются в процессы пищеварения и всасывания
В целом в органах брюшной полости отмечается относительно интенсивный кровоток, а кислородиз притекающей артериальной крови экстрагируется только на 15-20% В целом состояние, изображенное на рис 8-6, В, соответствует сосудистому руслу органов брюшной полости, и симпатическая иннервация играет существенную роль в его регуляции Артерии и вены всех органов брюшной полости богато иннервированы симпатическими сосудосуживающими нервами Максимальная активация симпатических сосудосуживающих нервов может привести к уменьшению на 80% кровотока в органах брюшной полости, а также к значительному перемещению крови из органов брюшной полости в центральный венозный пул У человека значительная часть крови, мобилизованная из кровотока органов брюшной полости при повышенной симпатической активации, поступает в результате сокращения вен печени Во многих других случаях селезенка функционирует как значительный резервуар, из которого кровь мобилизуется в результате опосредованного симпатическими нервами сокращения гладкой мускулатуры, локализующейся в наружной капсуле органа
Почечный кровоток
Почки в норме получают около 20% минутного объема в покое, и поскольку данная величина может уменьшиться практически до нуля, то регуляция почечного кровотока является важной для процесса регуляции деятельности всей сердечно-сосудистой системы Однако так как почки являются небольшими по своим размерам органами, изменения объема крови, заключенного в почках, не существенны для кровообращения в сердечно-сосудистой системе в целом
Хотя сосудистое русло почек является во многих отношениях специализированным, что представляется важным для функций почек (например, два последовательных раздельных капиллярных русла), но почечный кровоток принципиально регулируется так, как показано на рис 8-6В Увеличение симпатической сосудосуживающей активности может существенно снизить общий почечный кровоток в результате усиления нейрогенного тонуса почечных резистивных сосудов В действительности экстремальные состояния, приводящие к интенсивной и длительной активной симпатической вазоконстрикции, могут привести к развитию почечной недостаточности
позволяет поддерживать практически неизменный почечный кровоток при широком диапазоне показателей артериального давления, т е. почки обладают очень строгой системой ауторегуляцией Механизм, ответственный за процесс ауторегуляции почечного кровотока, до сих пор не установлен Были выдвинуты аргументы миогенной, метаболической гипотезы, а также для теории тканевого давления
Однако трудно представить, каким образом значительная метаболическая обратная связь может существовать в органе, в котором в норме кровоток существенно превышает метаболические потребности ткани Крайне незначительно выраженная реактивная гиперемия или ее отсутствие в почках также является аргументом против существенного влияния локальных сосудорасширяющих факторов на почечные артериолы
Механизмы, ответственные за внутренние процессы регуляции почечного кровотока и функцию почек, в настоящее время не установлены В то время как результаты некоторых исследований предполагают, что простагландины и в какой-то степени внутрипочечная ренин-ангиотензиновая система могут участвовать в данном процессе, в целом система локальной регуляции внутрипочечного кровообращения остается совершенно неизвестной
Сама функция почек обладает колоссальной важностью для деятельности сердечно сосудистой системы в целом, как это будет описано в главе 10
Кровоток в коже
Метаболическая активность клеток организма продуцирует тепло, которое должно отдаваться, чтобы температура тела оставалась постоянной Кожа является основной зоной организма, где происходит теплообмен с окружающей средой Изменения кожного кровотока в ответ на различные изменения метаболизма и внешней среды являются основным механизмом поддержания температурного гомеостаза (Другие механизмы, такие как мышечная дрожь, потоотделение и одышка, также принимают участие в регуляции температуры тела в экстремальных ситуациях)
Кожный кровоток, который составляет <5коло 6% от величины минутного объема крови в покое, может сократиться до1 / от его нормальной величины, если возникает необходимость сбережения тепла (например, при низкой температуре окружающей среды, в определенных фазах развития лихорадочной реакции) Напротив, кровоток в коже может увеличиться в 7 раз по сравнению с нормальным значением при необходимости увеличения теплоотдачи (например, при высокой температуре окружающей среды, при интенсивном метаболизме, после лихорадки)
Анатомические связи между микрососудами кожи высокоспециализированы и исключительно сложны Разветвленная сеть соединенных между собой вен, называемая венозным сплетением, в норме содержит основную часть объема располагающейся в коже крови, которые у индивидуумов с незначительной пигментацией кожи придают коже красноватый оттенок В значительной степени отдача тепла кровью в окружающее пространство осуществляется через обширную площадь венозных сплетений Венозные сплетения богато иннервированы симпатическими сосудосуживающими нервами При активации данных волокон кровь перемещается из венозных сплетении, что позволяет снизить теплоотдачу и приводит к побледнению кожи Поскольку кожа представляет собой один из кречнейп их > > >г т > ре тате спазма ье нозных сосудов значительная масса крови можег, с mccti 1 м в цс >атьн1 И'еноз ный пул
Кожные резистивные сосуды также богато иннервированы симпатическими сосудосуживающими нервами и, поскольку данные волокна обладают нормальной тонической активностью, сосуды кожи, регулирующие сопротивление, в норме обладают высоким нейрогенным тонусом. В целом кровоток в коже соответствует вариантам реакций, представленным на рис. 8-6, В Когда температура тела поднимается выше нормы, кровоток в коже рефлекторно возрастает. В определенных зонах (таких, как кисти рук, уши и нос) вазодилатация возникает исключительно вследствие исчезновения симпатического сосудосуживающего тонуса. В других областях (таких, как лоб, предплечья, подбородок, шея и передняя поверхность груди) расширение сосудов кожи, возникающее по мере согревания тела, существенно превышает то, которое отмечается просто при устранении симпатического сосудосуживающего тонуса.
Такая «активная» вазодилатация тесно связана с началом процесса потоотделения в данных зонах. Потовые железы в коже человека иннервируются холинергическими симпатическими волокнами, которые освобождают ацетилхолин. Стимуляция этих нервов вызывает потоотделение и одновременно выраженное расширение сосудов кожи. Конкретный механизм данной кожной вазодилатации, связанной с потоотделением, остается неясным, так как она не устраняется средствами, блокирующими сосудистые эффекты ацетилхолина
Длительное время считалось, что данная реакция вызывается локальным образованием брадикинина, вторичным по отношению к активации потовыхжелез. Есть данные, что вместо этого механизма холинергические симпатические нервы, оканчивающиеся в потовых железах, могут освобождать не только ацетилхолин, но и неадренергический, нехолинергический (НАНХ) сосудорасширяющий комедиатор, который в настоящее время еще не идентифицирован В то время как эти специальные симпатические нервы являются очень важным фактором для регуляции температуры тела, они не принимают участия в нормальной постоянной регуляции деятельности сердечно-сосудистой системы
Помимо рефлекторной реакции на изменения температуры тела, кожные сосуды также реагируют на местную температуру кожи В целом локальное охлаждение ведет к местному сужению сосудов, а местное повышение температуры вызывает локальное расширение сосудов Конкретные механизмы этой реакции не известны Если кисть руки погрузить в ледяную воду, то первоначально возникает почти полное прекращение кровотока в данной зоне, сочетающееся с сильной болью. Через несколько минут кровоток в конечности начинает увеличиваться, достигая величин, существенно превышающих нормальные значения, температура конечности возрастает и боль исчезает. Этот феномен называется холодовой вазодилатацией При продолжающемся воздействии кровоток в кисти руки циклически меняется каждые несколько минут, колеблясь от периода практически полного отсутствия кровотока до периода вазодилатации Механизм холодовой вазодилатации не известен, но предполагается, что норадреналин утрачивает свою способность суживать сосуды по мере того, как их температура снижается до О °C Независимо от конкретного механизма холодовая вазодилатация, очевидно, защищает ткани от повреждения холодом
При повреждении тканей в результате ожогов, ультрафиолетовой радиации, обморожения, контакта с агрессивными веществами и механической травмы возникает ответная реакция кровотока кожи Классическая реакция называется тройным ответом и возникает после энергичного проведения по коже острым предметом. Первым компонентом данной тройной реакции является появление красной полосы спустя примерно 15 с непосредственно вдоль участка кожи, которого коснулся острый предмет. Вскоре после этого яркая гиперемия с нечеткими границами появляется примерно на протяжении 2 см по сторонам от первичной полосы.
вдоль линии повреждения возникает валик Механизмы тройной реакций не известны, но представляется, что освобождение гистамина из поврежденных клеток, по крайней мере, частично обусловливает расширение сосудов по ходу красной полосы и последующее появление отека в виде валика Разлитая гиперемия свидетельствуете вовлечении в реакцию нервов в виде некого местного аксон-рефлекса, поскольку гиперемия появляется немедленно после перерезки кожных нервов, но не возникает после того, как периферические участки перерезанных нервов подвергаются дегенерации.
Легочный кровоток
Интенсивность кровотока через легкие во всех случаях равняется величине минутного объема. Когда при физической нагрузке минутный объем увеличивается, например, в три раза, то легочный кровоток тоже должен возрасти в три раза. В то время как кровоток через системный орган определяется его сосудистым сопротивлением (Q=AP/R), кровоток через легкие просто зависит от минутного объема сердца (Q=MO). Легочные сосуды в то же время в действительности обладают некоторым сопротивлением. Хотя величина сосудистого сопротивления в легких обычно не влияет на легочный кровоток, она является важным фактором, так как является одним из компонентов, определяющих величину давления в легочной артерии (&P=QxR). Напомним, что среднее давление в легочной артерии составляет около 13 мм рт ст., в то время как среднее системное артериальное давление равняется примерно 100 мм рт. ст Причина различия в величинах между системным и легочным артериальным давлением заключается не в том, что правое сердце слабее, чем левое, но скорее в том, что сопротивление сосудов легких исходно гораздо ниже общего периферического сосудистого сопротивления. В сосудистой системе легких сопротивление гораздо ниже, поскольку диаметр ее сосудов сравнительно больше
Очень важное различие между системными и легочными артериями и артериолами заключается в том, что легочные сосуды^в своей стенке содержат меньшее количество мышечных элементов и они более растяжимы. Когда легочное артериальное давление возрастает, легочные артерии и артериолы увеличиваются в диаметре.
Таким образом, увеличение давления в легочной артерии приводит к снижению сопротивления сосудов легких. Этот феномен является чрезвычайно важным, так как он ограничивает рост давления в легочной артерии, что происходит при увеличении минутного объема сердца
Наиболее важной активной реакцией сосудов легких является гипоксический спазм легочных артериол. Вспомним, что системные артериолы расширяются, реагируя на низкое значение Ро2. Механизм, который вызывает противоположную реакцию легочных сосудов, остается неясным. На современном уровне знаний предполагается, что локальный синтез простагландинов может принимать участие в реакции гипоксического спазма сосудов в легких Независимо от конкретного механизма гипоксический спазм сосудов весьма важен для эффективного легочного газообмена, поскольку он переориентирует кровоток из недостаточно вентилируемых областей легких Соответственно наилучшим образом вентилируемые области легких также получают максимальный кровоток. Преимущественно вследствие гипоксического спазма артериол, общая гипоксия организма (как например, на большой высоте над уровнем моря) вызывает увеличение сопротивления легочных сосудов и легочную артериальную гипертензию.
Как легочные артерии, так и вены иннервируются симпатическими сосудосуживающими волокнами, но рефлекторные влияния на легочные сосуды представляются гораздо менее важными, чем физические воздействия или локальная гипоксия. Для сердечно-сосудистой системы легочные вены являются функциональным резервуаром крови, и симпатическая вазоконстрикция легочных вен может быть существенной для мобилизации данного объема крови при общих стрессовых состояниях сердечнососудистой системы.
Следствием низкого среднего давления в легочных артериях является низкое гидростатическое давление в легочных капиллярах, составляющее около 8 мм рт. ст. (по сравнению с 25 мм рт ст в системных капиллярах) Поскольку онкотическое давление плазмы в легочных капиллярах составляет около 25 мм рт. ст , как и во всех капиллярах, то появляется желание сделать вывод, что транскапиллярные силы в легких будут вызывать постоянную реабсорбцию жидкости Тем не менее, это не так, поскольку легкие, как и другие ткани, постоянно продуцируют некоторое количество лимфы, для образования лимфатической жидкости требуется существование результирующей капиллярной фильтрации Это возможно, несмотря на необычно низкий уровень гидростатического давления в легочных капиллярах, поскольку интерстициальная жидкость легких содержит белок в необычно высокой концентрации, что обусловливает высокое онкотическое давление
Начало легочного кровообращения при рождении. Газообмен плода целиком осуществляется в плаценте, а кровообращение у плода полностью минует легкие. Кровьне поступает в легочную артерию, так как сосудистое сопротивление в спавшихся легких плода является очень высоким Правое и левое сердце плода фактически функционирует параллельно, прогоняя кровь через системные органы и плаценту. Как показано на рис 8-8, А, кровь плода, возвращающаяся из системных органов и плаценты, заполняет и правое, и левое сердце одновременно из-за наличия в межпредсердной перегородке отверстия, которое называется овальным окном
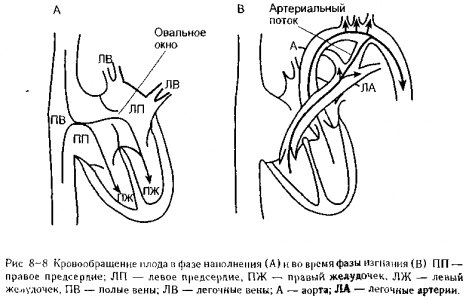
Кровь плода, которая нагнетается правым сердцем, не поступает в нефункционирующее сосудистое русло легких, а направляется в аорту через сосудистое соединение между легочной артерией и аортой, которое называется артериальным протоком (рис. 8-8, А).
С началом легочной вентиляции при рождении возникает резкое падение величины сосудистого сопротивления в легких. Это событие позволяет крови начать поступать в легкие из легочной артерии, что вызывает снижение легочного артериального давления.
Между тем общее системное сосудистое сопротивление значительно возрастает из-за прекращения кровотока через плаценту. Это приводит к увеличению давления в аорте, что тормозит движение крови через артериальный проток или делает его направление противоположным. Благодаря механизмам, которые в настоящее время не до конца ясны, но совершенно отчетливо связаны с увеличением напряжения кислорода в крови, артериальный проток постепенно спазмируется и полностью закрывается в течение промежутка времени, в норме составляющего от нескольких часов до нескольких дней
Изменения кровообращения, которые возникают при рождении, одновременно увеличивают постнагрузку давлением на левое сердце и уменьшают постнагрузку правого сердца. Косвенным образом это вызывает увеличение давления в левом предсердии по сравнению с правым предсердием, так что градиент давления для кровотока через овальное окно изменяется. Обратный поток крови через овальное окно в то же время предотвращается створками клапана на стороне овального окна обращенной в левое предсердие. В норме овальное окно, в конце концов, закрывается в результате непрерывного роста фиброзной ткани.